El virus Nipah representa uno de los patógenos más preocupantes de nuestro tiempo. Con una tasa de mortalidad promedio del 70% y capacidad de transmisión entre personas, este paramixovirus zoonótico ha captado la atención de la comunidad científica mundial como un modelo para la preparación ante pandemias. Pero, ¿qué sabemos realmente sobre este virus? ¿De dónde viene y por qué está emergiendo con mayor frecuencia?

Orígenes Naturales: Una Historia Evolutiva Milenaria
Contrario a teorías conspirativas que puedan circular, el virus Nipah tiene un origen completamente natural y bien documentado. Los paramixovirus, la familia viral a la que pertenece Nipah, son patógenos antiguos que han coevolucionado con sus huéspedes durante millones de años. Esta familia viral incluye patógenos conocidos como el virus del sarampión, las paperas y los virus de la parainfluenza humana, todos con historias evolutivas extensas y bien caracterizadas.
Los murciélagos del género Pteropus, conocidos como “zorros voladores”, han sido los huéspedes naturales de henipaviruses durante milenios. Estos mamíferos voladores, distribuidos naturalmente a través del sudeste asiático y el sur de Asia, mantienen el virus en sus poblaciones sin desarrollar enfermedad severa, un equilibrio evolutivo típico entre patógenos y sus reservorios naturales. El virus Nipah no fue “creado” recientemente; simplemente permaneció circulando silenciosamente en poblaciones de murciélagos hasta que los cambios ambientales y la expansión humana crearon las condiciones perfectas para su detección y salto a otras especies.
El Descubrimiento: Malasia 1998-1999
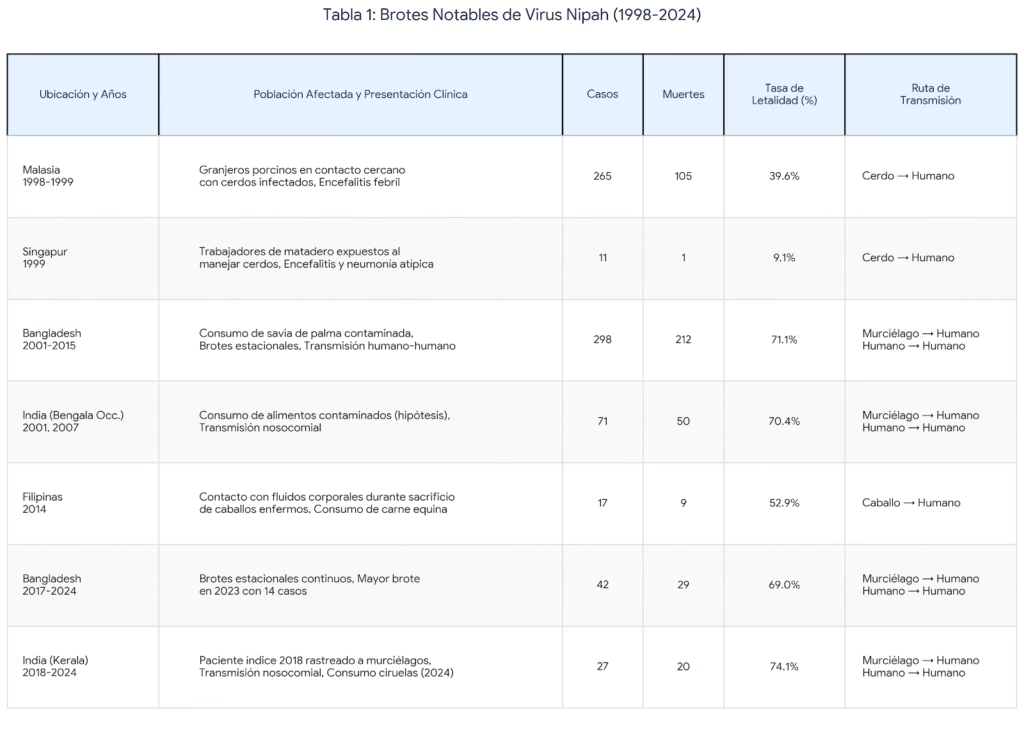
La primera identificación del virus Nipah ocurrió entre 1998 y 1999 durante un brote devastador en granjas porcinas de Malasia. Este evento marca el momento en que la comunidad científica tomó conocimiento del virus, no su “creación” o aparición súbita. Durante este brote inicial, 265 personas se infectaron y 105 murieron, principalmente granjeros que tenían contacto estrecho con cerdos infectados.
¿Qué provocó esta emergencia? La respuesta yace en factores ecológicos completamente naturales. La deforestación masiva en Malasia había destruido los hábitats naturales de los murciélagos Pteropus, forzándolos a buscar alimento en áreas cultivadas cerca de granjas porcinas. Los murciélagos, naturalmente portadores del virus, contaminaron frutas parcialmente consumidas que posteriormente fueron ingeridas por los cerdos. Los cerdos actuaron como “huéspedes puente”, amplificando el virus antes de transmitirlo a los trabajadores agrícolas.
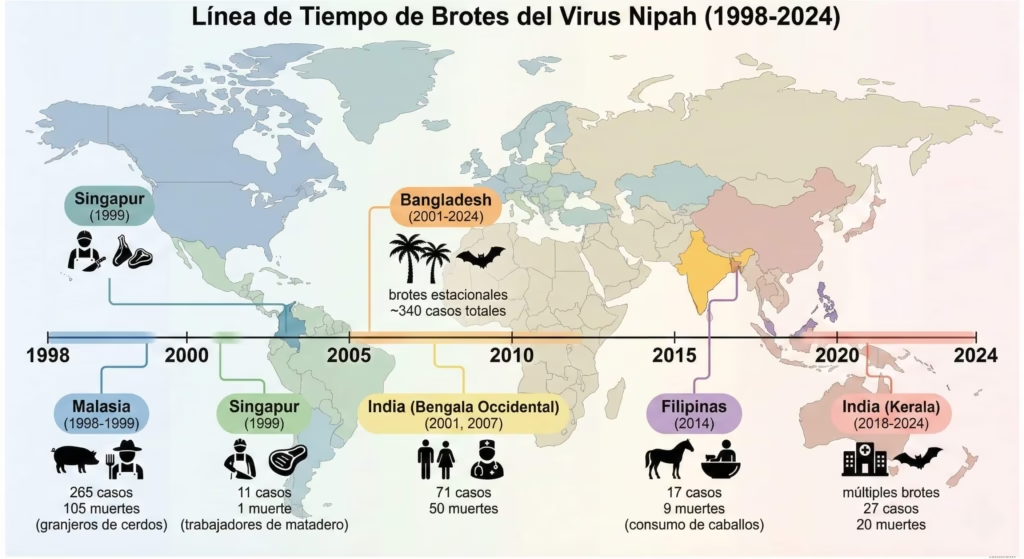
La conexión Singapur-Malasia también fue crucial: trabajadores de mataderos en Singapur se infectaron al manejar cerdos importados de las granjas malayas afectadas, resultando en 11 casos y 1 muerte. Este patrón de transmisión – murciélago→cerdo→humano – estableció el paradigma clásico de emergencia zoonótica natural.
Patrones de Transmisión: La Complejidad de un Salto Zoonótico Natural
El virus Nipah ejemplifica perfectamente cómo los patógenos pueden saltar naturalmente entre especies a través de múltiples rutas:
Transmisión Directa Murciélago-Humano
En Bangladesh e India, la ruta de transmisión más documentada involucra el consumo de savia fresca de palma datilera contaminada por murciélagos infectados. Los murciélagos Pteropus medius, la única especie de Pteropus presente en estas regiones, se alimentan naturalmente de esta savia durante la noche. Su saliva y orina, que contienen el virus durante períodos de excreción, contaminan la savia que posteriormente consumen los humanos sin tratamiento térmico.
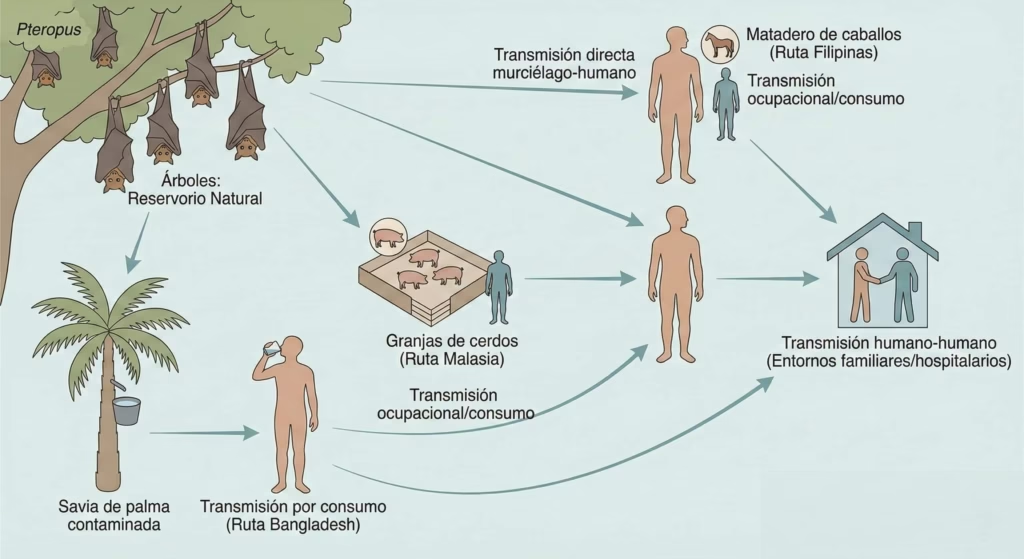
Huéspedes Puente Variables
Además de los cerdos en Malasia, otros animales domésticos pueden actuar como intermediarios. En Filipinas (2014), caballos infectados transmitieron el virus a humanos durante su sacrificio y consumo. Estudios serológicos han detectado anticuerpos contra Nipah en ganado bovino, cabras, perros y gatos en áreas endémicas, sugiriendo exposición natural a henipavirus relacionados.
Transmisión Persona-a-Persona
Una característica particularmente preocupante del virus Nipah es su capacidad para transmitirse entre humanos, principalmente a través de secreciones respiratorias. Los estudios epidemiológicos muestran que aproximadamente el 10% de los pacientes transmiten el virus a otras personas, y dentro de este grupo, cerca del 10% son “súper-propagadores” que infectan a más de cinco individuos.
La Biología Molecular: Entendiendo la Maquinaria Viral
Estructura y Clasificación Taxonómica
El virus Nipah pertenece al orden Mononegavirales, caracterizado por genomas de ARN de cadena sencilla negativa no segmentados. Dentro de la familia Paramyxoviridae, Nipah se clasifica en el género Henipavirus, junto con el virus Hendra (HeV) y otros henipavirus emergentes como el virus Langya.
Los paramixovirus comparten una arquitectura genómica conservada que incluye seis genes principales organizados linealmente: nucleocápside (N), fosfoproteína (P), proteína matriz (M), proteína de fusión (F), proteína de unión (G para henipavirus, H o HN para otros paramixovirus), y la ARN polimerasa dependiente de ARN o proteína grande (L). Esta organización genómica representa millones de años de evolución viral optimizada.
Ciclo de Replicación del Paramixovirus: Desde la Unión hasta la Gemación
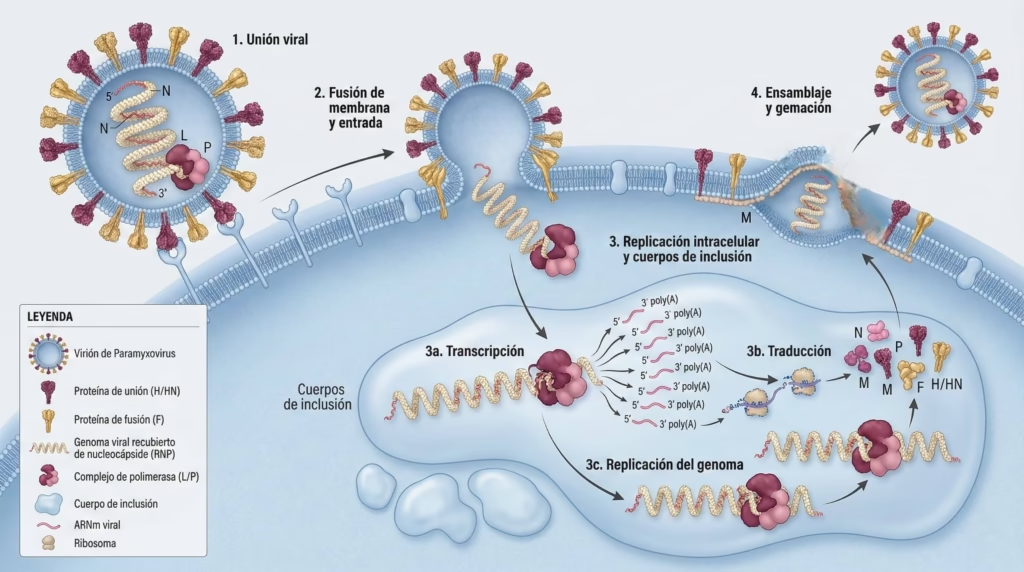
El Complejo de Replicación: Una Maquinaria Molecular Sofisticada
Investigaciones recientes utilizando criomicroscopía electrónica han revelado la estructura tridimensional del complejo polimerasa del virus Nipah con una resolución de 2.9 Å. Este complejo L-P (polimerasa grande-fosfoproteína) es fundamental para la replicación viral y representa un objetivo terapéutico prometedor.
La proteína L del virus Nipah contiene múltiples dominios funcionales: el dominio N-terminal (NTD), el dominio de ARN polimerasa dependiente de ARN (RdRp), y el dominio PRNTasa (poliribonucleotidiltransferasa). La fosfoproteína P forma estructuras tetraméricas estabilizadas por una “caperuza” α-helicoidal, creando una interfaz de unión de 3,466 Ų con la proteína L.
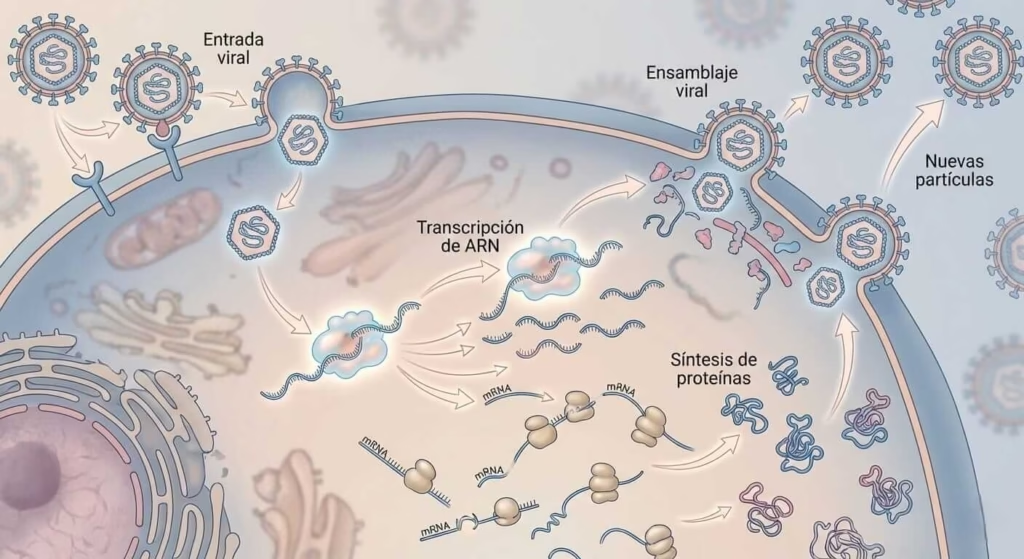
Esta arquitectura molecular no surgió de la nada; representa la culminación de procesos evolutivos que han optimizado la replicación viral en células de mamíferos durante eones. La similitud estructural con otros miembros del orden Mononegavirales confirma su origen evolutivo compartido.
Diversidad Genética y Evolución Regional
Linajes Virales y Distribución Geográfica
Los análisis filogenéticos han identificado tres a cuatro linajes principales del virus Nipah, dependiendo de los criterios de clasificación utilizados. Esta diversidad genética refleja la larga historia evolutiva del virus en diferentes poblaciones de murciélagos a través de Asia.
Los virus secuenciados de los extremos occidentales (India) pertenecen al linaje 1A, también reportado en Bangladesh. Los virus de los extremos orientales (Indonesia y Malasia) pertenecen al linaje 2A. Los países intermedios muestran una mezcla de linajes diferentes, con Camboya exhibiendo la mayor diversidad genética viral, sugiriendo una circulación histórica extensa o mayor diversidad de especies huésped en esta región.
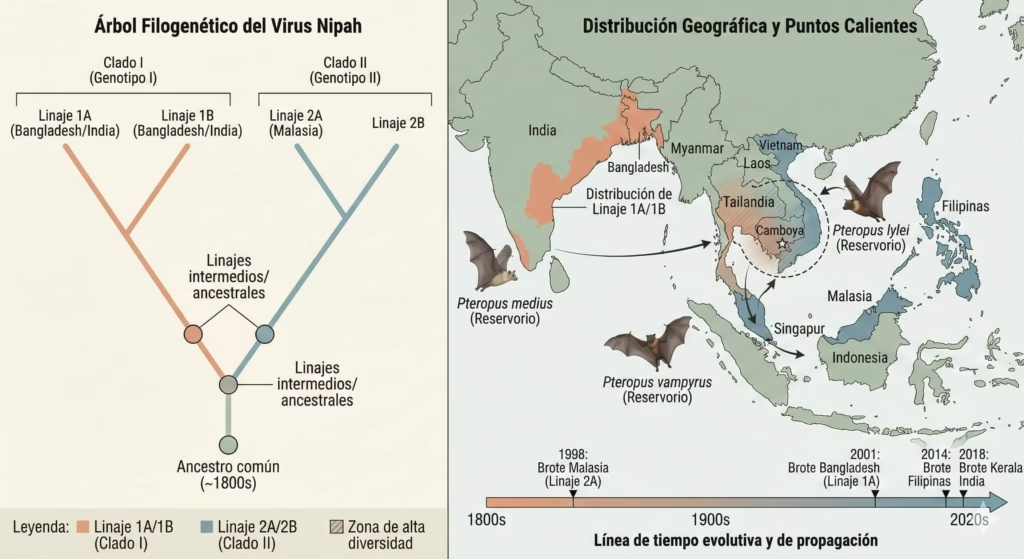
Coexistencia de Múltiples Linajes
Un hallazgo fascinante es la cocirculación de diferentes linajes virales dentro del mismo refugio de murciélagos simultáneamente, con un promedio de dos linajes por refugio. Las secuencias de ARN viral muestran una fuerte estructura espacial que correlaciona con ubicaciones geográficas específicas, con movimiento geográfico limitado del virus.
Esta diversidad genética no indica manipulación artificial, sino procesos evolutivos naturales típicos de virus de ARN. La presencia de múltiples linajes cocirculantes puede ofrecer mayor diversidad viral y, por tanto, mayor potencial para que variantes superen barreras específicas de huésped o transmisión.
Factores Ecológicos de Emergencia: Cuando los Mundos Colisionan
Deforestación y Fragmentación del Hábitat
La emergencia del virus Nipah está intrínsecamente ligada a cambios antropogénicos en el paisaje. En Malasia, la deforestación extensiva para plantaciones de palma aceitera y desarrollo urbano destruyó los hábitats forestales naturales de los murciélagos Pteropus. Esta pérdida de hábitat forzó a los murciélagos a buscar fuentes alimentarias alternativas en áreas periurbanas y agrícolas.
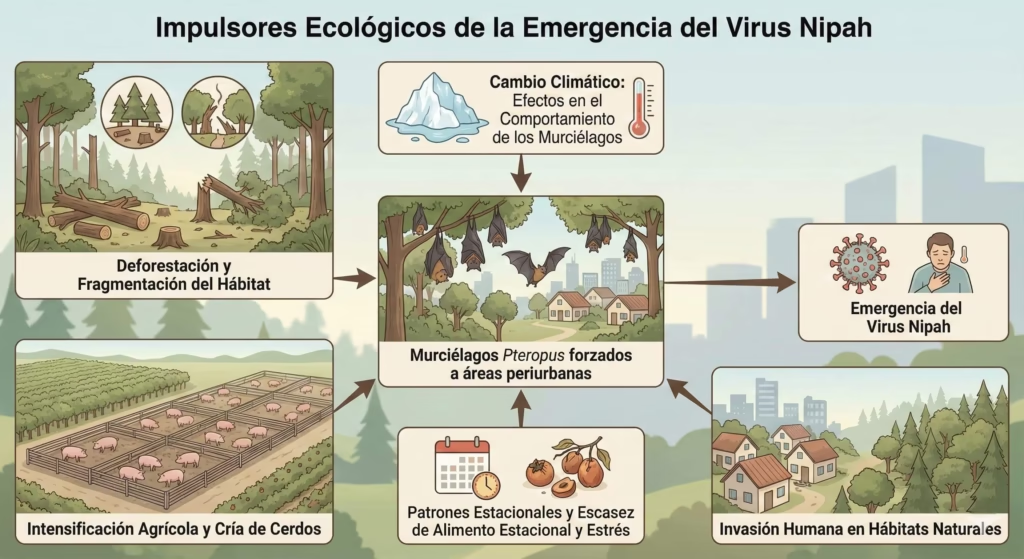
En Bangladesh, aunque la deforestación ocurrió históricamente hace cientos de años, las poblaciones contemporáneas de murciélagos son pequeñas, fragmentadas y viven en estrecha asociación con comunidades humanas cerca de fuentes alimentarias cultivadas. Esta proximidad facilita la transmisión viral.
Kerala, India, está experimentando deforestación rápida, y su impacto en las poblaciones locales de murciélagos permanece poco estudiado. Es posible que condiciones similares a las observadas en la emergencia del virus Hendra en Australia – como cambios en el uso del suelo combinados con eventos climáticos – estén impulsando la emergencia del virus Nipah en Kerala.
Estrés Nutricional y Excreción Viral
Los estudios del virus Hendra en Australia han demostrado que la pérdida de alimento nativo lleva a los murciélagos a alimentarse en hábitats subóptimos. Se ha propuesto que el estrés nutricional puede reducir el control inmunológico del virus, una teoría respaldada por la observación de que los murciélagos excretan múltiples virus en pulsos sincrónicos junto con Hendra durante períodos de alto riesgo de derrame, como los inviernos cuando es probable que experimenten escasez alimentaria.
Cambio Climático y Patrones Estacionales
Los henipavirus muestran patrones estacionales distintivos de excreción. En Australia subtropical, los picos estacionales de excreción del virus Hendra ocurren generalmente durante el invierno, con variación interanual sustancial. Los picos de excreción son más altos en poblaciones en hábitats subóptimos nuevos y después de que los animales han experimentado escasez alimentaria.
En contraste con Hendra, las detecciones del virus Nipah han sido limitadas a través del muestreo transversal de refugios de murciélagos, con detecciones longitudinales similarmemente limitadas. Sin embargo, al igual que Hendra, una mayor prevalencia de excreción se ha asociado con derrames. El muestreo de refugios de murciélagos en respuesta a derrames recientes de Nipah en humanos ha sido la estrategia más exitosa para detectar el virus.
Manifestaciones Clínicas: Un Espectro de Gravedad
Presentación Clínica Variable
La infección por virus Nipah puede manifestarse como enfermedad respiratoria, encefalitis rápidamente progresiva y severa, o ambas. Durante el brote malayano de 1998-1999, los signos clínicos distintivos entre granjeros porcinos infectados incluían mioclonus segmentario (contracciones musculares), arreflexia e hipotonía (ausencia de reflejos y tono muscular disminuido), hipertensión y taquicardia, sugiriendo compromiso del tronco encefálico y la médula espinal cervical superior.
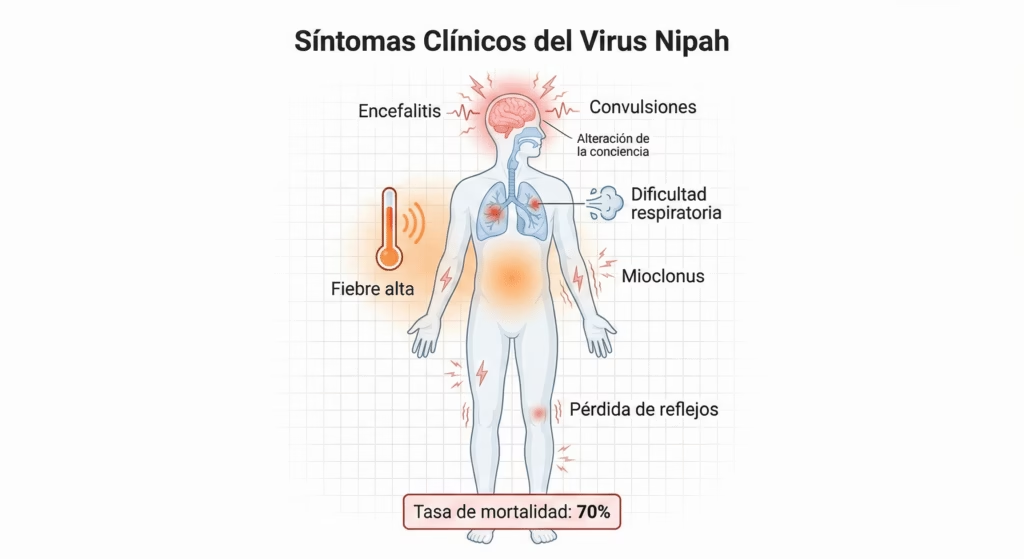
Las características clínicas durante brotes en Bangladesh entre 2001 y 2004 incluyeron fiebre, estado mental alterado, cefalea, tos, dificultad respiratoria, vómito y convulsiones. Durante el brote de 2023 en Kerala, todos los pacientes exhibieron síntomas de fiebre, tos, disnea y convulsiones.
Variabilidad Regional en Síntomas
La variabilidad sintomática entre brotes resalta la necesidad de entender mejor los factores moleculares, virológicos, regionales y poblacionales que impulsan síntomas clínicos diferenciales en áreas de brote. Esta variación puede reflejar diferencias en linajes virales, factores del huésped, o rutas de exposición.
Respuesta Inmune y Correlatos de Protección
Establecimiento de Correlatos de Protección
Investigaciones recientes en primates no humanos han establecido correlatos de protección para candidatos vacunales contra Nipah. Utilizando el modelo estándar dorado de monos verdes africanos, los estudios han determinado umbrales específicos de anticuerpos protectores:
Para el linaje de Bangladesh (NiVB):
- Anticuerpos de unión: >1,100 unidades
- Anticuerpos neutralizantes: FRNT50 >60
Para el linaje de Malasia (NiVM):
- Anticuerpos de unión: >800 unidades
- Anticuerpos neutralizantes: FRNT50 >80
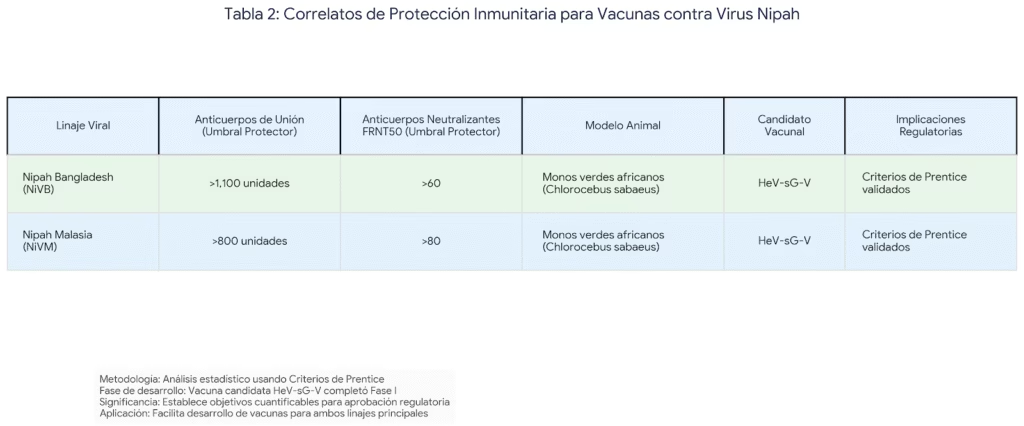
Estos correlatos, establecidos utilizando criterios estadísticos de Prentice, proporcionan objetivos cuantificables para el desarrollo vacunal y tienen implicaciones regulatorias importantes para la aprobación de vacunas candidatas.
Respuestas Innatas en Murciélagos
Los estudios en modelos celulares de murciélagos han revelado mecanismos fascinantes de control viral. La proteína antiviral tetherina suprime la replicación del virus Nipah en células de murciélago. La estimulación con interferón-α pan upregula los transcritos de tetherina, y la inhibición de la expresión de tetherina usando ARN de interferencia pequeño lleva a una pérdida completa de la restricción mediada por tetherina de la replicación de Nipah.
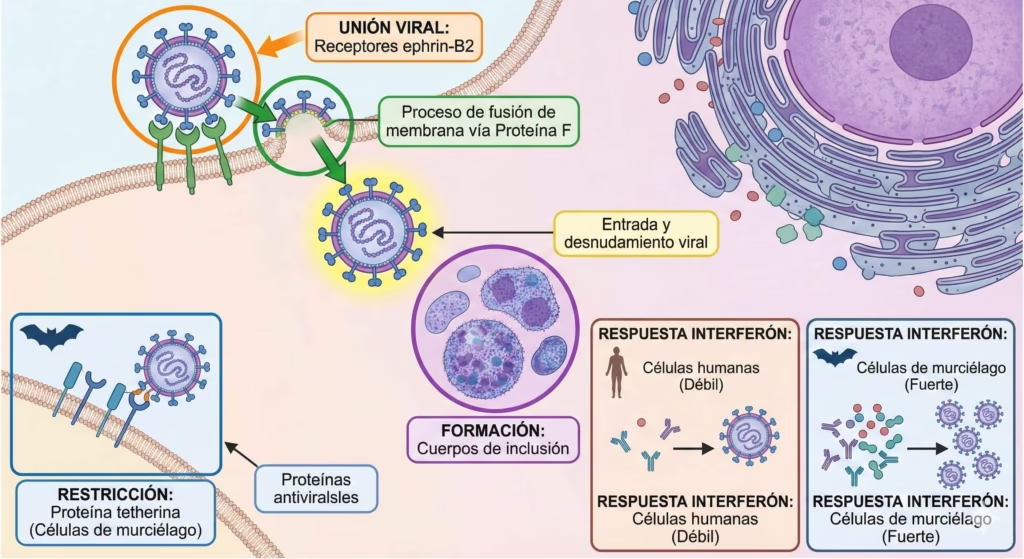
Paradójicamente, la infección con aislados de Nipah de Bangladesh y Malasia en células pulmonares de Pteropus alecto no indujo la expresión de interferón tipo I ni genes antivirales estimulados por interferón canónicos, sugiriendo que la infección por Nipah en estas células de murciélago puede suprimir respuestas antivirales mediadas por interferones tipo I.
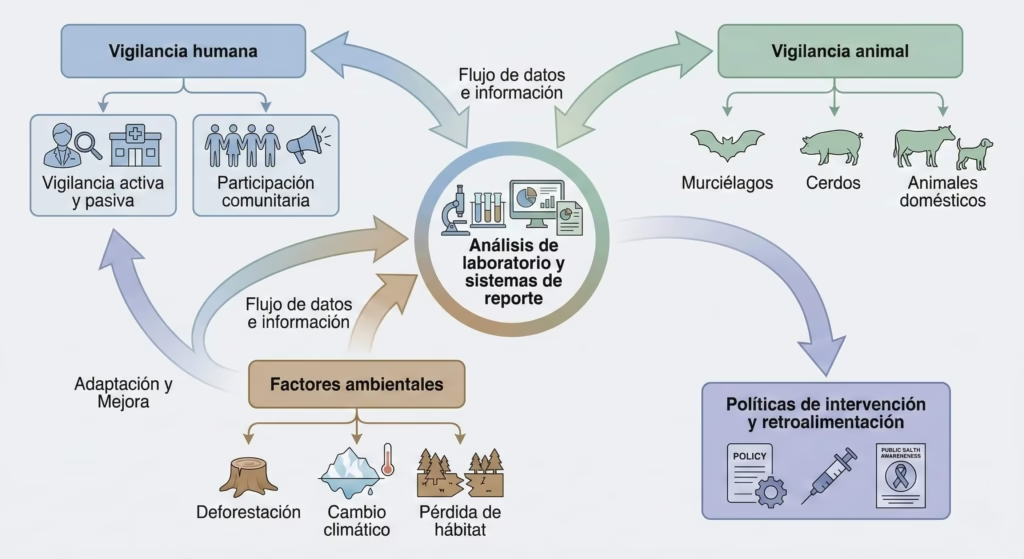
Vigilancia y Estrategia One Health
Implementación de Vigilancia Integrada
El enfoque One Health reconoce la interconexión entre salud humana, animal y ambiental. Para el virus Nipah, esto significa implementar sistemas de vigilancia que monitoreen simultáneamente:
En Humanos:
- Vigilancia activa: detección regular de anticuerpos y ARN viral en poblaciones de alto riesgo
- Vigilancia pasiva: monitoreo de casos inusuales o muertes, reporte de casos sospechosos y confirmados
- Participación comunitaria y análisis de datos de vigilancia
En Animales:
- Cerdos: monitoreo de salud en granjas porcinas, vigilancia serológica y molecular
- Animales domésticos: vigilancia en caballos, cabras, ovejas, gatos y perros en regiones que se superponen geográficamente con poblaciones de murciélagos pteropódidos
- Murciélagos: captura y recolección de muestras para análisis, vigilancia de condición corporal, estado nutricional y reproductivo, seroprevalencia de anticuerpos contra Nipah y presencia de ARN viral
Integración de Datos y Modelado Predictivo
La integración de datos de vigilancia humana y animal, junto con la identificación de hotspots ecológicos para futura emergencia de Nipah, permitirá desarrollar modelos predictivos más robustos. Estos sistemas integrados son esenciales para la detección temprana y respuesta rápida a brotes.
Intervenciones y Prevención: Lecciones de Bangladesh
Soluciones Simples pero Efectivas
El conocimiento sobre la ruta de transmisión del virus Nipah de murciélagos a savia de palma datilera a humanos en Bangladesh ha llevado al desarrollo de soluciones simples pero efectivas. El uso de “faldones” de bambú en ollas de barro para prevenir que los murciélagos accedan a la savia de palma datilera es un método efectivo para prevenir la contaminación con Nipah.
Una intervención de comunicación para el cambio de comportamiento también ha sido probada, donde mensajes como “no beber savia cruda” y “solo savia segura” han resultado en mayor conocimiento público y menor exposición a savia potencialmente contaminada con Nipah.
Medidas de Control de Infecciones
Durante brotes, las medidas estrictas de control de infecciones son críticas:
- Precauciones universales en entornos hospitalarios
- Equipo de protección personal apropiado para trabajadores de salud
- Aislamiento de pacientes confirmados y sospechosos
- Protocolos de desinfección y higiene de manos
- Identificación temprana y aislamiento de casos sintomáticos
Desafíos y Brechas en el Conocimiento
Modelos Animales Limitados
Una limitación significativa en la investigación del virus Nipah es la falta de modelos animales apropiados. No todas las especies de murciélagos son susceptibles a la infección experimental con Nipah. Rousettus aegyptiacus no es susceptible a infección experimental, mientras que Pteropus poliocephalus, una especie australiana que no se sabe que mantenga Nipah naturalmente, desarrolla infección subclínica cuando se infecta subcutáneamente.
Dinámicas de Transmisión Poco Claras
Permanece poco claro cómo los refugios individuales pueden sostener cadenas de transmisión de múltiples linajes y cómo interactúan los linajes. La presencia de múltiples linajes cocirculantes puede ofrecer mayor diversidad viral y, por tanto, mayor potencial para que una variante supere barreras de huésped puente o humano dentro del huésped para el derrame.
Factores de Excreción Viral
Los factores intrínsecos y extrínsecos que afectan la excreción viral en murciélagos permanecen poco comprendidos. Establecer colonias de murciélagos susceptibles al virus permitirá estudios de transmisión horizontal y vertical, así como factores como cortisol, reproducción, ambiente y temperatura que afectan la excreción viral.
Implicaciones para la Preparación ante Pandemias
Nipah como Patógeno Modelo
La Organización Mundial de la Salud identifica al virus Nipah como patógeno prioritario debido a su alta tasa de mortalidad y capacidad de transmisión persona-a-persona, representando riesgo pandémico. La ubicación geográfica de brotes identificados de Nipah continúa expandiéndose, incluyendo a Kerala, el sitio de la muerte reciente de un estudiante de 24 años en septiembre de 2024.
Lecciones para Otras Zoonosis
Como muchas enfermedades infecciosas humanas emergentes tienen origen animal, estas enfermedades zoonóticas pueden representar una amenaza severa para la seguridad sanitaria global y la economía. El brote reciente de virus Marburg en Rwanda y el brote generalizado continuo de mpox desde 2022 son ejemplos de brotes zoonóticos emergentes donde un mejor entendimiento de derrames podría ayudar a desarrollar intervenciones.
Direcciones Futuras: Investigación y Colaboración
Necesidades de Investigación Prioritarias
- Estudios longitudinales de poblaciones de murciélagos en Kerala para investigar cómo responden al cambio ambiental continuo
- Desarrollo de modelos celulares adicionales derivados de murciélagos, incluyendo líneas celulares primarias e inmortalizadas y organoides
- Establecimiento de colonias de murciélagos en cautiverio de especies conocidas como reservorios de Nipah
- Plataformas multi-ómicas para identificar mecanismos de excreción y derrame viral

Colaboración Internacional
El enfoque One Health requiere colaboración multisectorial a niveles nacionales e internacionales. Las organizaciones cuadripartitas de las Naciones Unidas (FAO, PNUMA, OIE y OMS) están enfatizando cada vez más los enfoques One Health. La importancia del compromiso comunitario como aspecto crucial para la implementación exitosa de enfoques One Health en la mitigación de riesgos asociados con derrames zoonóticos en áreas de alto riesgo no puede subestimarse.

Conclusión: Preparándose para un Futuro Incierto
El virus Nipah representa un paradigma perfecto de cómo los patógenos naturales pueden emerger y amenazar la salud global en nuestra era de cambio ambiental acelerado. Su historia – desde la circulación silenciosa en murciélagos durante milenios hasta su reconocimiento como amenaza pandémica – ilustra la complejidad de las enfermedades zoonóticas emergentes.
La clave para manejar futuras amenazas de Nipah y patógenos similares radica en:
- Comprensión científica robusta de los mecanismos de derrame zoonótico
- Sistemas de vigilancia integrados que monitoreen la interfaz humano-animal-ambiente
- Preparación comunitaria con intervenciones culturalmente apropiadas
- Colaboración internacional bajo el marco One Health
- Inversión sostenida en investigación y desarrollo de contramedidas
El virus Nipah nos recuerda que en nuestro mundo interconectado, la salud humana está inextricablemente ligada a la salud de los ecosistemas que compartimos. Solo a través de enfoques holísticos y colaborativos podremos anticipar, prevenir y responder efectivamente a las amenazas zoonóticas emergentes que seguramente enfrentaremos en las décadas venideras.
La naturaleza no conspira contra nosotros; simplemente sigue sus propias reglas evolutivas. Nuestra responsabilidad es entender esas reglas y adaptar nuestro comportamiento en consecuencia, respetando los equilibrios ecológicos mientras protegemos la salud pública global.
LISTA COMPLETA DE REFERENCIAS
- Yadav, P.D. et al. A One Health approach to understanding and managing Nipah virus outbreaks. Nature Microbiology 10, 1272–1281 (2025). https://doi.org/10.1038/s41564-025-02020-9
- Structure of the Nipah virus polymerase phosphoprotein complex. Nature Communications 15, Article number: 8234 (2024). https://doi.org/10.1038/s41467-024-52701-y
- Establishing an immune correlate of protection for Nipah virus in nonhuman primates. npj Vaccines 9, Article number: 204 (2024). https://doi.org/10.1038/s41541-024-01036-2
- Duprex, W.P., Dutch, R.E. Paramyxoviruses: Pathogenesis, Vaccines, Antivirals, and Prototypes for Pandemic Preparedness. The Journal of Infectious Diseases 228(Supplement_6), S390–S397 (2023). https://doi.org/10.1093/infdis/jiad123
- Baron, S. (editor). Structure and Classification of Viruses. In: Medical Microbiology. 4th edition. Galveston (TX): University of Texas Medical Branch; 1996. Chapter 41. Available from: https://www.ncbi.nlm.nih.gov/books/NBK8174/
- World Health Organization. Nipah Virus Infection—India. Disease Outbreak News. 3 October 2023. https://www.who.int/emergencies/disease-outbreak-news/item/2023-DON490
VIDEO
AVISO IMPORTANTE
La información contenida en este artículo tiene únicamente propósitos educativos e informativos. No constituye consejo médico, diagnóstico o tratamiento profesional. Siempre consulte a un médico calificado o profesional de la salud para cualquier pregunta relacionada con condiciones médicas específicas.
Esta información se basa en investigación científica publicada y fuentes académicas confiables, pero la ciencia está en constante evolución. Las recomendaciones de salud pública pueden cambiar según nuevos descubrimientos.
El autor no se hace responsable por el uso que se haga de esta información ni por las consecuencias derivadas de su aplicación.