¿Qué son los GLP-1 y por qué importan?
Los agonistas del receptor de GLP-1 (GLP-1 RA) son una clase de medicamentos que imitan la acción del péptido similar al glucagón tipo 1, una hormona intestinal liberada después de comer. Su mecanismo incluye estimular la secreción de insulina dependiente de glucosa, inhibir el glucagón, retrasar el vaciamiento gástrico y reducir el apetito a nivel central.
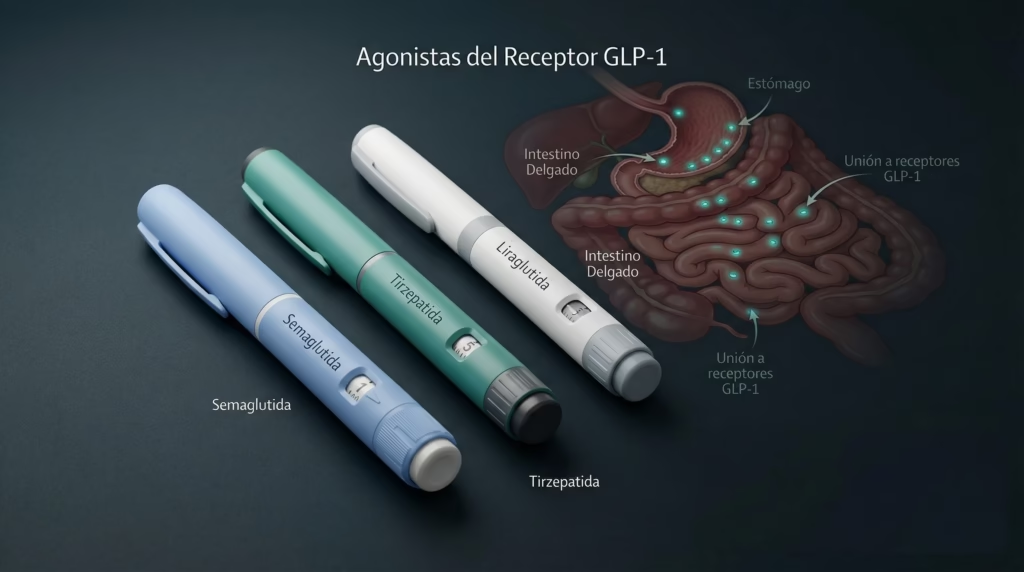
Originalmente aprobados para el tratamiento de la diabetes tipo 2, estos medicamentos han transformado el campo de la medicina de la obesidad en los últimos años. El semaglutide (Wegovy, Ozempic), el liraglutide (Saxenda) y el tirzepatide (Mounjaro, Zepbound) —este último un agonista dual GLP-1/GIP— han demostrado pérdidas de peso de entre 10 y 22% del peso corporal en ensayos clínicos de fase 3. En diciembre de 2025, la FDA aprobó la primera formulación oral de un GLP-1 para obesidad, lo que amplía aún más el acceso a esta clase de medicamentos.
El mercado global de estos fármacos se estima en 70 mil millones de dólares actualmente y podría alcanzar 201 mil millones para 2033.
El problema que nadie menciona con suficiente frecuencia

Con la atención puesta en los beneficios —pérdida de peso, reducción de riesgo cardiovascular, mejora del control glucémico—, un aspecto de la terapia con GLP-1 recibe menos atención de la que merece: la pérdida de masa magra.
Cuando alguien pierde peso, no pierde exclusivamente tejido adiposo. Pierde una combinación de grasa, masa magra (músculo, órganos, hueso, líquidos) y agua. Esta realidad fisiológica aplica a cualquier intervención de pérdida de peso: dieta, ejercicio, cirugía bariátrica o farmacoterapia.
La pregunta relevante no es si se pierde masa magra —eso ocurre en todos los casos—, sino cuánta se pierde, si es proporcional a la pérdida de peso, y si afecta la función muscular.
¿Cuánta masa magra se pierde con GLP-1?
Los datos de los ensayos clínicos principales muestran lo siguiente:
En el ensayo STEP-1 con semaglutide 2.4 mg semanal, un subgrupo de 140 pacientes se sometió a absorciometría de rayos X de energía dual (DXA) antes y después de 68 semanas de tratamiento. El peso corporal disminuyó en promedio 15.3 kg, de los cuales 6.92 kg correspondieron a masa magra. Esto representa el 45.2% del peso perdido proveniente de masa magra.
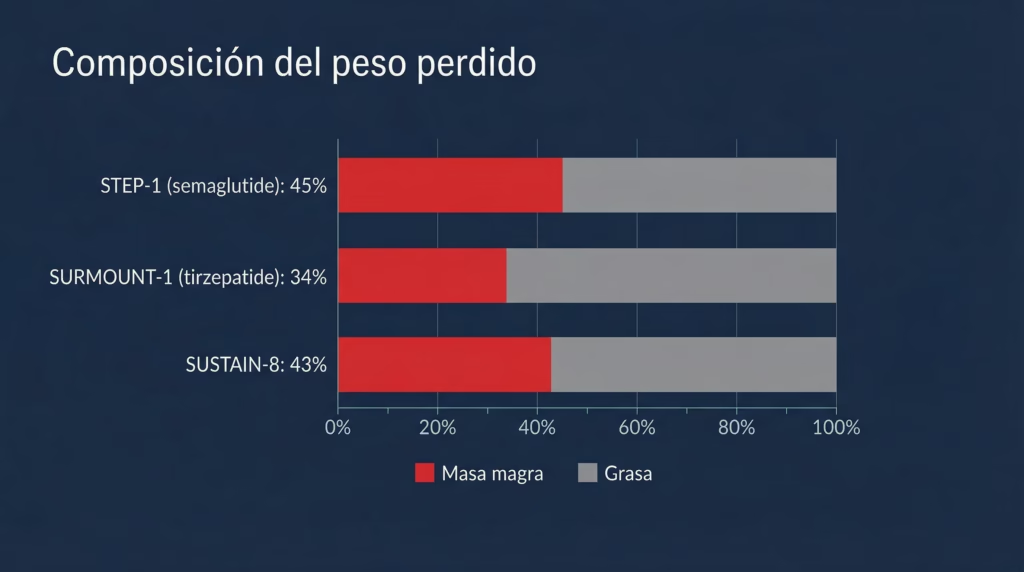
En SURMOUNT-1 con tirzepatide, la pérdida de masa magra fue de 5.67 kg sobre una pérdida total de 22.1 kg, lo que equivale al 34.3% de masa magra.
En un subestudio del ensayo SUSTAIN-8 con semaglutide en pacientes con diabetes tipo 2, la fracción de masa magra perdida fue del 43.4%.
Un meta-análisis publicado en Metabolism en 2024, que analizó 22 estudios con 2,258 participantes, encontró que en promedio el 25% del peso perdido con GLP-1 RA corresponde a masa magra. El liraglutide fue el único agente de la clase sin pérdida estadísticamente significativa de masa magra en ese análisis.
Estos números parecen elevados. Pero requieren contexto.
El matiz más importante: masa magra ≠ músculo
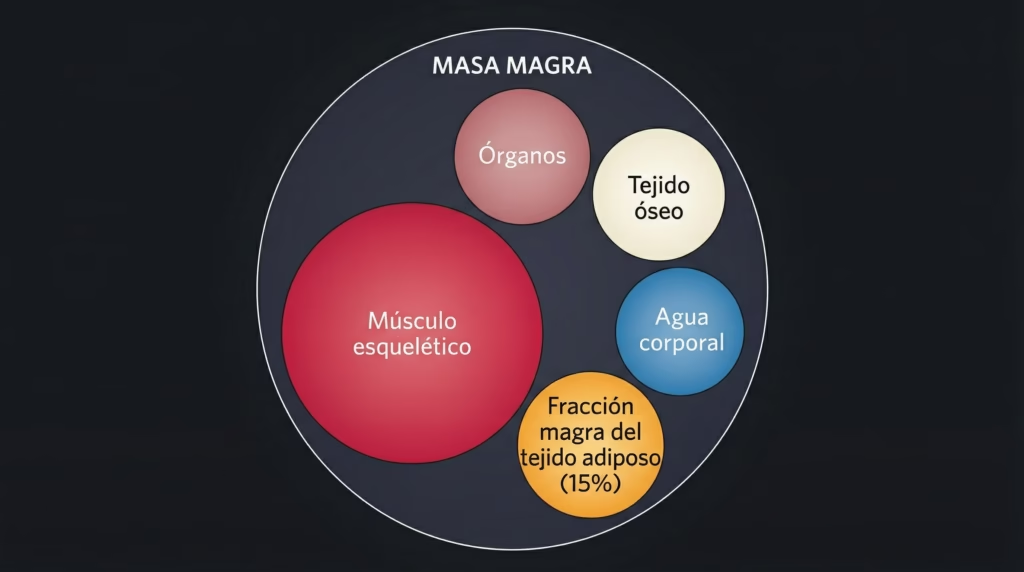
Este es el punto que más frecuentemente se pasa por alto en la comunicación pública sobre estos medicamentos.
La masa magra es una medida compuesta. Incluye músculo esquelético, pero también tejido óseo, órganos internos, agua corporal total, y un componente que pocos mencionan: hasta el 15% del tejido adiposo está compuesto por masa libre de grasa. Esto significa que una pérdida sustancial de grasa por sí sola producirá cierta reducción en la masa magra medida por DXA, sin que el músculo real haya disminuido.
La herramienta estándar en los ensayos clínicos —el DXA— no puede distinguir con precisión estos componentes. Los estudios que han utilizado resonancia magnética (RM) ofrecen una imagen más precisa.
Dos estudios con RM —uno con liraglutide y otro con tirzepatide (subestudio SURPASS-3 MRI)— midieron el z-score de volumen muscular: un índice que compara el volumen muscular individual con lo esperado para alguien del mismo sexo y tamaño corporal. Los cambios encontrados fueron comparables con la pérdida muscular esperada por envejecimiento normal y por la magnitud de pérdida de peso alcanzada. No se observó pérdida excesiva.
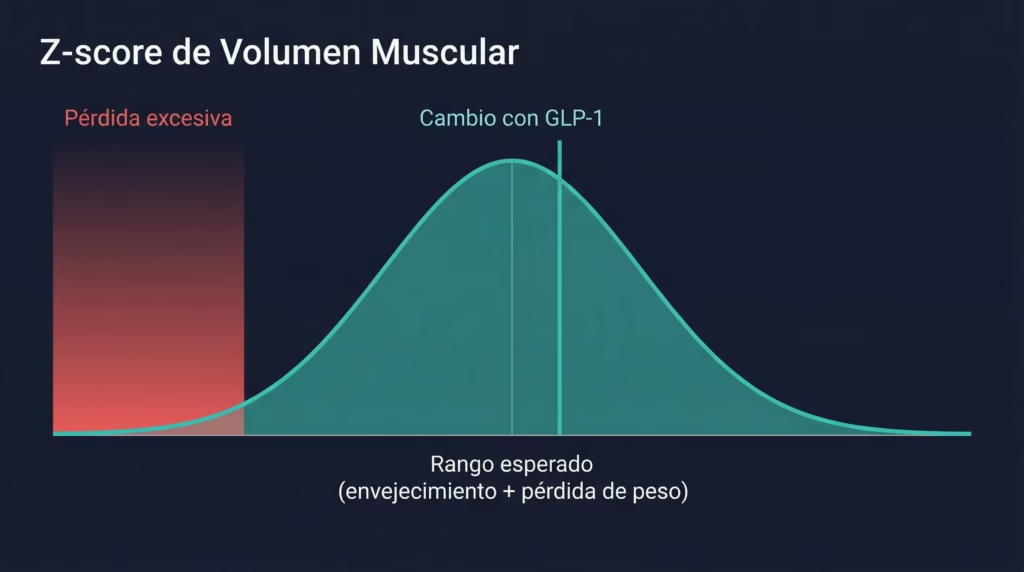
Adicionalmente, ambos estudios reportaron una reducción en la infiltración de grasa intramuscular —un marcador de calidad muscular— en los grupos tratados. Esto sugiere que la calidad del músculo remanente mejoró.
La conclusión provisional de la evidencia más reciente: los cambios en masa muscular con GLP-1 parecen ser adaptativos, no maladaptativos, en la mayoría de los pacientes estudiados. Sin embargo, esta conclusión proviene de poblaciones relativamente jóvenes (edad media 45-55 años) y no necesariamente aplica a todos los grupos.
Poblaciones con mayor riesgo
La evidencia general puede ser tranquilizadora en promedio, pero ciertos grupos presentan un riesgo más elevado de sarcopenia clínicamente relevante durante el tratamiento con GLP-1.
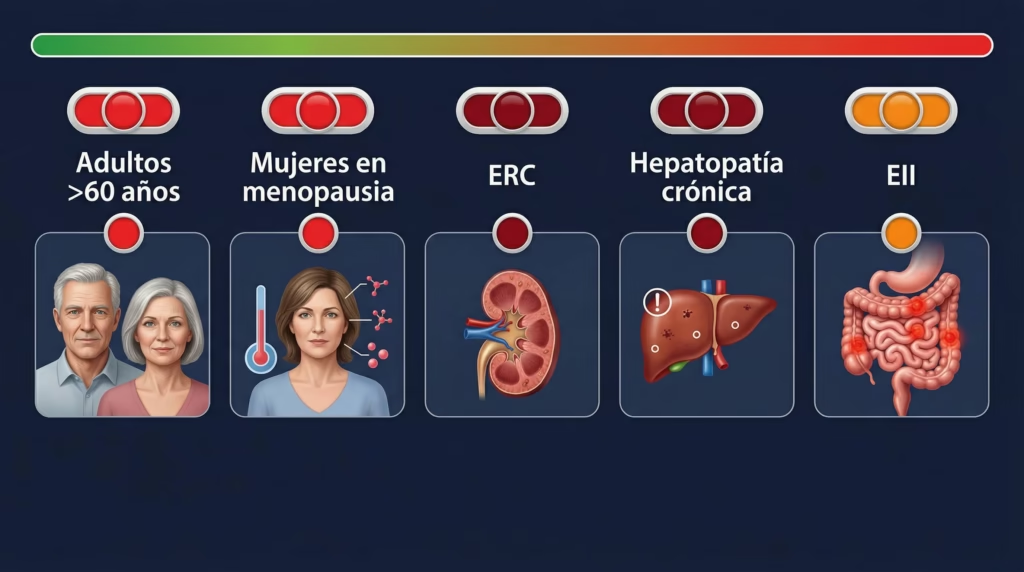
Adultos mayores. A partir de los 40 años, el músculo esquelético disminuye entre 1 y 2% anual, con pérdidas aceleradas después de los 60. Estudios señalan que las pérdidas de masa magra observadas en algunos ensayos con GLP-1 (a lo largo de 68-72 semanas) equivalen a 20 años de pérdida muscular relacionada con el envejecimiento. Los adultos mayores también presentan resistencia anabólica: responden menos al estímulo de proteína y ejercicio para sintetizar músculo. Los ensayos principales de estos medicamentos excluyeron en su mayoría a personas mayores de 75 años, por lo que los datos en este grupo son escasos.
Mujeres en menopausia o perimenopausia. El descenso en estradiol y testosterona reduce la síntesis proteica muscular y aumenta la deposición de grasa visceral. Más del 60-70% de los participantes en los ensayos STEP y SURMOUNT fueron mujeres, pero ninguno midió niveles hormonales basales. Se desconoce si el estado menopáusico modifica la magnitud de pérdida muscular.
Pacientes con enfermedad renal crónica (ERC). La prevalencia de sarcopenia en ERC es de aproximadamente 40%, y de 26% en pacientes en diálisis. La restricción proteica clásicamente recomendada para frenar la progresión de la ERC —entre 0.55 y 0.80 g/kg/día— está directamente en tensión con los requerimientos proteicos necesarios para preservar músculo. El semaglutide y el tirzepatide excluyeron pacientes con ERC significativa en sus ensayos de pérdida de peso.
Pacientes con hepatopatía crónica. En cirrosis, la sarcopenia se asocia con casi el doble de riesgo de mortalidad, según un meta-análisis de 22 estudios con aproximadamente 7,000 pacientes. Los datos sobre el efecto de los GLP-1 en la composición muscular en esta población son prácticamente inexistentes.
Pacientes con enfermedad inflamatoria intestinal (EII). La sarcopenia afecta a entre el 30 y el 50% de los pacientes con EII, secundaria a malabsorción, inflamación sistémica crónica y disbiosis. Aproximadamente el 15-40% de los pacientes con EII tienen obesidad, lo que hace al uso de GLP-1 relevante en este grupo, aunque no hay estudios específicos.
¿Por qué ocurre la pérdida de masa magra?
Los mecanismos son predominantemente indirectos, dado que los receptores de GLP-1 no se expresan en el músculo esquelético humano. El efecto sobre músculo no es directo: es consecuencia de los cambios metabólicos sistémicos que el fármaco produce.
El mecanismo principal es la reducción del apetito. Al disminuir la ingesta calórica total, disminuye también la ingesta de proteína. Estudios comparativos entre liraglutide y restricción calórica equivalente sugieren que los pacientes en GLP-1 tienden a desplazar su dieta hacia alimentos de menor densidad proteica. Cuando la disponibilidad de aminoácidos es insuficiente, el organismo recurre al músculo como fuente.
A nivel hormonal, la pérdida de peso rápida reduce los niveles de IGF-1 e insulina —dos señales anabólicas centrales para el mantenimiento muscular— mientras puede incrementar relativamente los niveles de cortisol, que tiene efectos catabólicos sobre el músculo.
La vía mTOR, central en la síntesis de proteína muscular, puede verse suprimida en el contexto de balance energético negativo sostenido. La restricción calórica aguda disminuye la tasa de síntesis proteica miofibrilar postprandial.
Por otra parte, hay mecanismos potencialmente protectores: los GLP-1 mejoran la sensibilidad a la insulina, que normalmente suprime la proteólisis muscular. También pueden promover la biogénesis mitocondrial en músculo esquelético y mejorar el flujo microvascular muscular, aunque estos efectos son más robustos en modelos animales que en humanos.
Estrategias con respaldo en evidencia

La buena noticia es que hay intervenciones concretas que reducen el riesgo de pérdida muscular significativa.
Proteína adecuada. Las guías bariátricas recomiendan un mínimo de 1.5 g/kg de peso ideal por día. Para adultos mayores, las guías ESPEN sugieren 1.2 a 1.5 g/kg/día, con énfasis en la distribución equitativa entre comidas para optimizar la síntesis proteica muscular a lo largo del día. La leucina —un aminoácido de cadena ramificada— es especialmente relevante: se necesitan aproximadamente 3 g de leucina por comida para activar de forma óptima la vía mTOR en adultos mayores. Cuando el apetito está reducido por el GLP-1, los suplementos líquidos de proteína son una alternativa práctica.
Entrenamiento de resistencia. Tanto el ejercicio aeróbico como el de resistencia ayudan a preservar masa muscular durante pérdida de peso. El entrenamiento de fuerza tiene la ventaja adicional de mejorar la función y la fuerza muscular, no solo el volumen. Una revisión sistemática demostró que el ejercicio puede preservar la masa libre de grasa durante restricción calórica en adultos con sobrepeso. Combinado con ingesta proteica adecuada, el efecto es mayor que con cualquiera de los dos por separado. Las guías recomiendan al menos dos sesiones de fuerza semanales; para adultos mayores, idealmente tres.
Suplementos. La evidencia más sólida, aunque no específica para usuarios de GLP-1, apunta a: omega-3 (EPA/DHA, 2-4 g/día), que reduce la inflamación y promueve la síntesis proteica muscular; vitamina D, cuya deficiencia se asocia con mayor prevalencia de sarcopenia; HMB (beta-hidroxi-beta-metilbutirato), metabolito de la leucina con efectos antiproteolíticos; y creatina, particularmente en adultos mayores bajo entrenamiento de resistencia.
Microbioma. Una revisión sistemática que incluyó 10 estudios clínicos y 26 preclínicos evaluó el efecto de probióticos (Lactobacillus y Bifidobacterium principalmente), prebióticos y trasplante fecal sobre la masa muscular. Los resultados sugieren un impacto positivo, aunque los datos en pacientes en GLP-1 son inexistentes. Consumir variedad de plantas (meta de 30 tipos distintos por semana) y reducir el picoteo frecuente también apoyan un microbioma más diverso.
El horizonte farmacológico
El campo está avanzando hacia combinaciones que permitan perder grasa sin comprometer músculo.
El bimagrumab es un anticuerpo monoclonal que bloquea el receptor de activina tipo II, impidiendo la acción de la activina A y la miostatina —señales que normalmente suprimen el crecimiento muscular. En un ensayo clínico de fase 2 en pacientes con obesidad y diabetes tipo 2, el bimagrumab redujo la masa grasa en 20.5% e incrementó la masa magra en 3.6% sin cambios en la ingesta calórica.
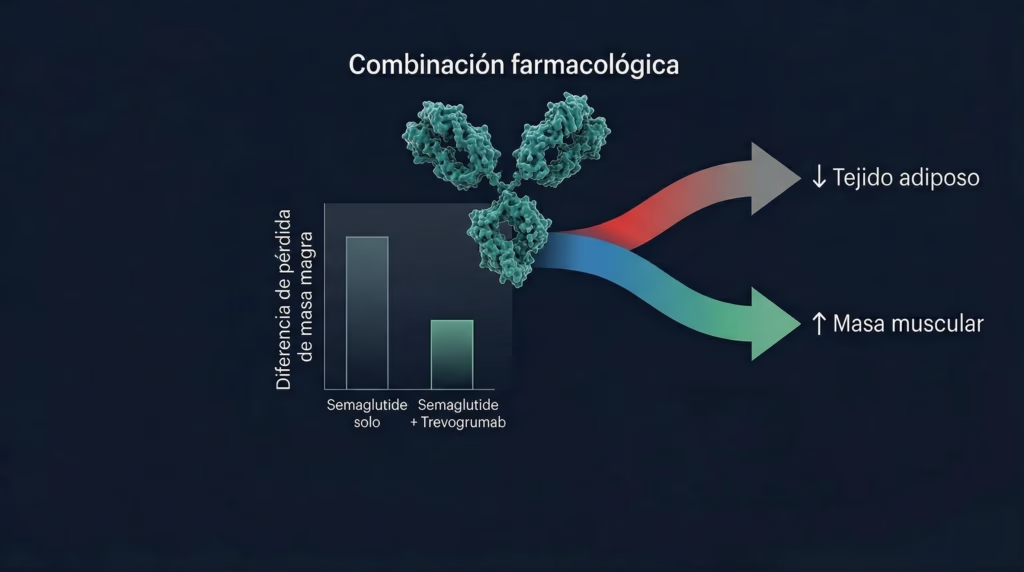
El ensayo COURAGE evaluó la combinación de trevogrumab (inhibidor de miostatina) con semaglutide. Resultados preliminares: el grupo combinado perdió 3.3% de masa magra frente al 6.5% del grupo en semaglutide solo. Una reducción aproximada del 50%.
Estudios en primates no humanos con inhibición de miostatina combinada con agonismo GLP-1 mostraron pérdida de grasa robusta con incremento de masa magra. Moléculas como el PTT-A —un triagonista en investigación— muestran pérdida de grasa sin pérdida muscular en modelos preclínicos.
El objetivo de estas combinaciones es claro: disociar la pérdida de grasa de la pérdida de músculo, permitiendo resultados metabólicos favorables sin el costo sobre la masa magra.
Monitoreo recomendado
Para pacientes y médicos, estas son las consideraciones prácticas:
Antes de iniciar GLP-1, es razonable evaluar la composición corporal de base (al menos con BIA o DXA si está disponible), especialmente en adultos mayores, personas con comorbilidades crónicas o baja actividad física basal.
Durante el tratamiento, el monitoreo de fuerza de prensión (grip strength) y la velocidad de marcha son indicadores funcionales simples y con valor pronóstico reconocido por las definiciones actuales de sarcopenia (EWGSOP2, SDOC). La masa magra medida por DXA sola no refleja completamente el estado muscular.
La evaluación nutricional regular —idealmente con un dietista familiarizado con terapia de obesidad— ayuda a garantizar que la ingesta proteica sea adecuada a pesar de la reducción del apetito.
Conclusión
Los GLP-1 producen pérdida de masa magra, un fenómeno documentado y cuantificado en los ensayos clínicos. La proporción varía entre 25 y 45% del peso perdido según el ensayo, aunque parte de esa cifra refleja reducción de componentes no musculares de la masa magra.
La evidencia más reciente, usando resonancia magnética, sugiere que los cambios en volumen muscular son adaptativos y proporcionales al envejecimiento esperado para la magnitud de pérdida de peso alcanzada, en las poblaciones estudiadas. La calidad muscular —medida como infiltración de grasa intramuscular— mejora con el tratamiento.
Sin embargo, ciertos grupos presentan mayor riesgo: adultos mayores, mujeres en menopausia, y pacientes con enfermedades crónicas como ERC, hepatopatía o EII. En estos grupos, la evidencia específica es escasa y la vigilancia es más necesaria.
Las intervenciones con mayor respaldo para mitigar el riesgo son: proteína suficiente (1.2-1.5 g/kg/día, bien distribuida), entrenamiento de resistencia regular, y consideración de suplementos selectivos (omega-3, vitamina D, leucina/HMB).
El futuro apunta a combinaciones farmacológicas que permitan maximizar la pérdida de grasa mientras se preserva o incluso incrementa la masa muscular.
Referencias
- Karakasis P, et al. Effect of GLP-1 receptor agonists and co-agonists on body composition. Metabolism. 2024.
- Linge J, et al. Muscle Mass and Glucagon-Like Peptide-1 Receptor Agonists: Adaptive or Maladaptive Response to Weight Loss? Circulation. 2024.
- Neeland IJ, Linge J, Birkenfeld AL. Changes in lean body mass with glucagon-like peptide-1-based therapies and mitigation strategies. Diabetes Obes Metab. 2024;26(Suppl. 4):16–27.
- Rossi AP, et al. Muscle loss and GLP-1R agonists use. Acta Diabetologica. 2025.
- Memel Z, et al. Impact of GLP-1 Receptor Agonist Therapy in Patients High Risk for Sarcopenia. Curr Obes Rep. 2025;14:63.
- Gatto NM, et al. The Effects of GLP-1 Agonists on Musculoskeletal Health and Orthopedic Care. Curr Rev Musculoskelet Med. 2025; PMC12325148.
- Ceasovschih A, et al. GLP-1 receptor agonists and muscle mass effects. Pharmacological Research. 2025.
Este contenido es de carácter educativo. No sustituye la evaluación médica individual. Consulta a tu médico antes de iniciar, modificar o suspender cualquier tratamiento.