El Descubrimiento que Podría Cambiarlo Todo
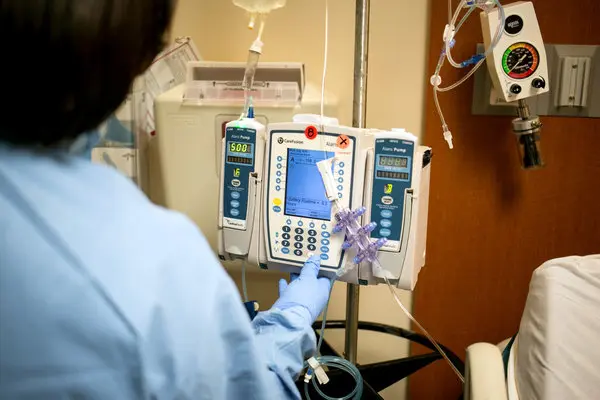
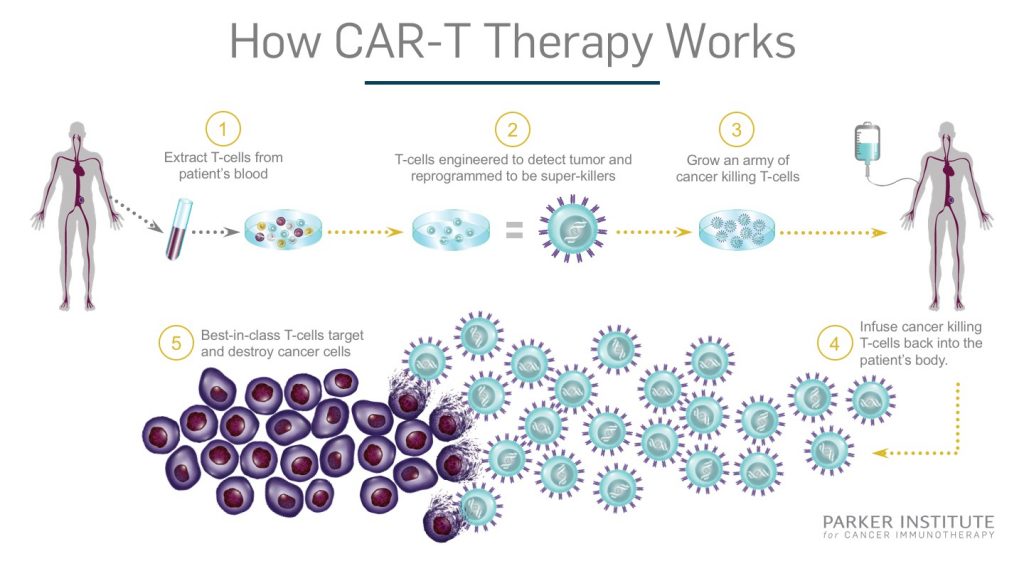
Las terapias CAR-T son una revolución contra el cáncer. Imagina que tomas tus propias células inmunes (células T), las modificas genéticamente para que reconozcan y ataquen el cáncer, y las reinyectas en tu cuerpo. Suena perfecto, ¿verdad?
El problema es que funcionan… pero no tan bien como quisiéramos. Y cuando digo “no tan bien”, me refiero a que tienen cuatro obstáculos principales que limitan su efectividad. Déjame explicarte cada uno como si te lo estuviera contando tomando un café.
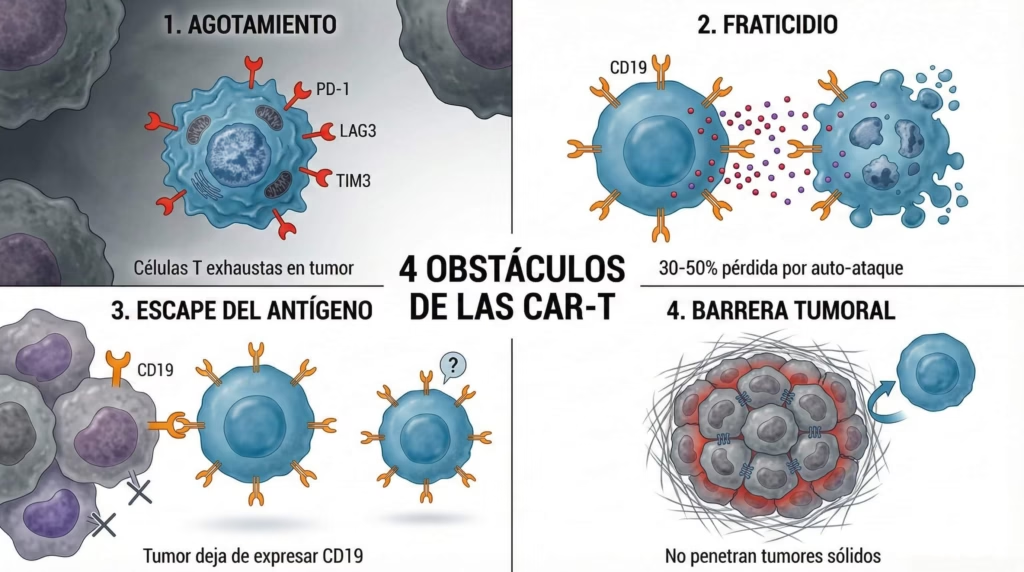
Primero está el agotamiento, o “exhaustion” como le dicen los científicos. Las CAR-T entran al tumor como soldados listos para pelear, pero el ambiente tumoral es como un maratón sin agua ni descanso. Las células T llegan con toda la energía, empiezan a atacar el cáncer, pero poco a poco se van agotando hasta que simplemente dejan de funcionar. Es frustrante porque las tienes ahí, dentro del tumor, pero ya no pueden hacer nada.
Luego viene algo todavía más extraño: el fraticidio. Sí, leíste bien. Las CAR-T se atacan entre sí. ¿Por qué? Porque están diseñadas para matar células con una proteína específica llamada CD19, que es común en ciertos tipos de cáncer. El problema es que ellas mismas expresan CD19 en su superficie. Entonces, una CAR-T ve a su compañera, detecta CD19, y la ataca. El resultado es que entre 30 y 50% de tus células CAR-T mueren antes siquiera de llegar al tumor. Es como un ejército que se dispara a sí mismo antes de la batalla.
El tercer problema es que el cáncer es muy listo. Si las CAR-T atacan células con CD19, el tumor simplemente deja de expresar CD19. Es como si cambiaras tu uniforme para que el enemigo no te reconozca. Este fenómeno se llama “escape del antígeno”, y es una de las razones principales por las que el cáncer regresa después de terapias CAR-T inicialmente exitosas.
Y finalmente, está el problema de los tumores sólidos. Las CAR-T funcionan bastante bien en leucemias y linfomas porque estos son cánceres “líquidos” que circulan en la sangre. Pero los tumores sólidos—como los de pulmón, mama, o colon—son como fortalezas con murallas impenetrables. Las CAR-T simplemente no logran entrar, y aunque algunas lo consigan, el ambiente dentro del tumor es tan hostil que se agotan inmediatamente.
La Solución: CELLFIE
Aquí es donde entra CELLFIE, y créeme que este avance es impresionante. Un equipo de científicos de Stanford se preguntó: ¿y si pudiéramos usar CRISPR para editar los genes de las CAR-T y hacerlas mejores? No solo eso, sino ¿y si pudiéramos probar miles de modificaciones diferentes para encontrar las combinaciones perfectas?
CELLFIE son las siglas de CRISPR-Enhanced Lentiviral Libraries For Immunotherapy Engineering. El nombre es complicado, pero el concepto es brillante. Es una plataforma que permite combinar la terapia CAR-T con edición genética CRISPR en un solo paso, y luego probar masivamente qué modificaciones funcionan mejor.
¿Cómo funciona CELLFIE?
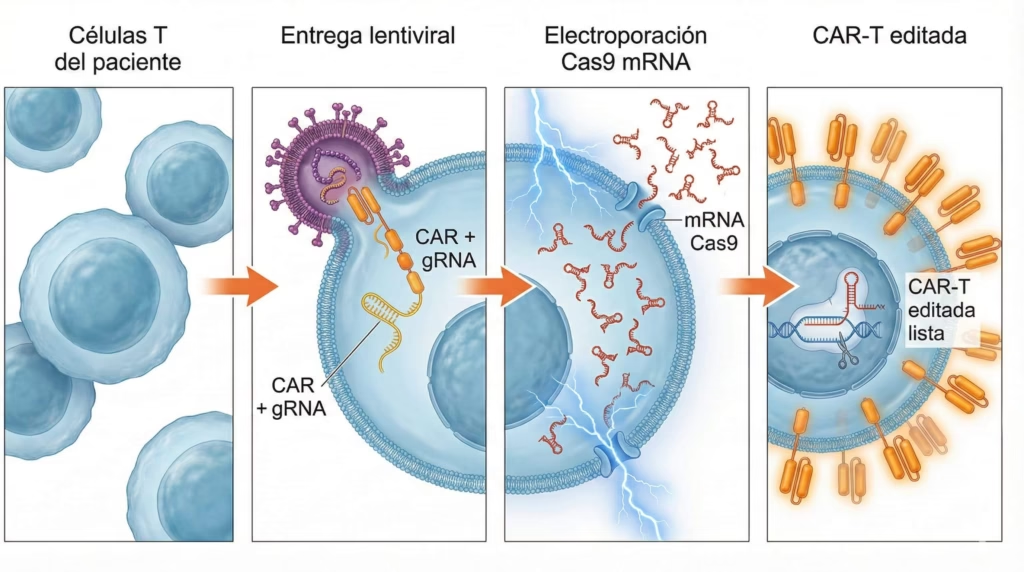
El sistema es ingenioso porque usa dos entregas separadas pero coordinadas. Primero, utilizan un virus modificado (lentivirus) que funciona como un camión de entrega. Este virus lleva dos cosas al mismo tiempo: el receptor CAR que va a reconocer el cáncer, y una guía CRISPR que funciona como un GPS molecular diciéndole a CRISPR exactamente qué gen debe editar.
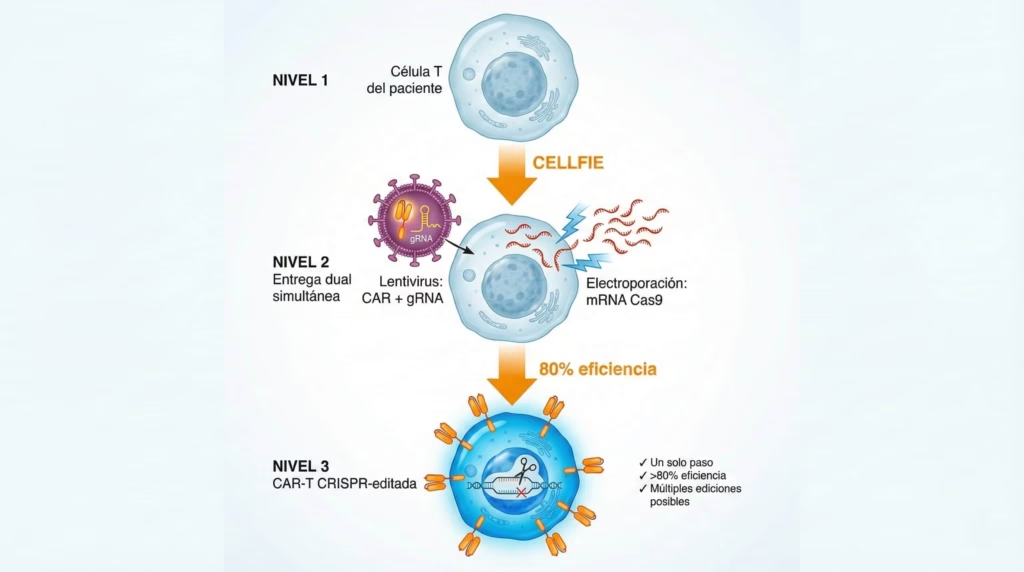
Luego viene la segunda parte. En lugar de usar otro virus para entregar Cas9 (las famosas “tijeras moleculares” de CRISPR), los investigadores decidieron ser más listos. Entregan Cas9 como ARN mensajero directamente a las células mediante electroporación. ¿Por qué es esto importante? Porque es mucho más barato y eficiente que usar virus adicionales. Además, el ARNm se degrada naturalmente después de hacer su trabajo, así que no permanece en las células para siempre.
El resultado es sorprendente: más del 80% de las células terminan con la modificación genética deseada. Y aquí viene lo mejor: este sistema no solo puede eliminar genes (knockout), sino que también puede hacer edición de bases—donde cambias letras específicas del ADN—o incluso activar genes que normalmente estarían apagados. Es como tener una navaja suiza molecular.
El Experimento: 58 Búsquedas Masivas
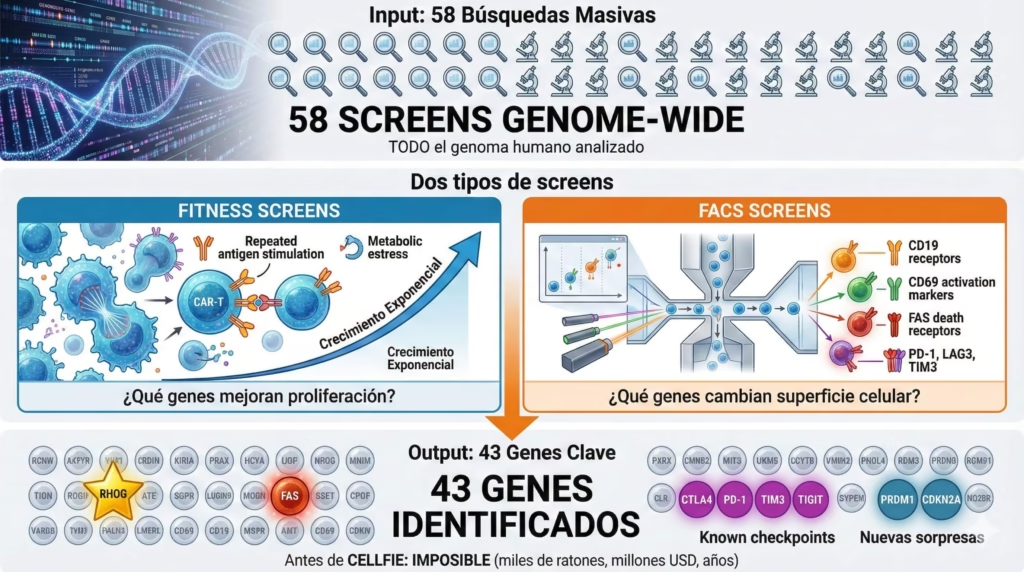
Con esta herramienta en mano, los investigadores hicieron algo que francamente parece sacado de ciencia ficción. Realizaron 58 búsquedas diferentes donde editaron prácticamente TODO el genoma humano para ver qué genes, cuando se eliminan o modifican, mejoran las CAR-T. Antes de CELLFIE, esto hubiera sido imposible. Literalmente. Habrían necesitado miles de ratones, millones de dólares, y años de trabajo.
Dividieron sus búsquedas en dos categorías principales. Las búsquedas de aptitud (fitness screens) buscaban genes que, al eliminarse, hacen que las CAR-T se multipliquen más o sobrevivan mejor cuando están bajo estrés, como cuando son estimuladas repetidamente con antígeno tumoral.
Las búsquedas FACS fueron aún más específicas. Usaron citometría de flujo para buscar genes que, al eliminarse, cambian proteínas específicas en la superficie celular. Por ejemplo, midieron CD19 para entender el fraticidio (trogocitosis), CD69 como marcador de activación, FAS como marcador de muerte celular, y los famosos checkpoints de agotamiento: PD-1, LAG3, y TIM3.
Al final identificaron 43 genes clave. Algunos eran los sospechosos habituales—los famosos checkpoints inmunes como CTLA4, PD-1, TIM3, y TIGIT que ya conocíamos de inmunoterapias previas. Pero encontraron sorpresas que nadie esperaba…
El Descubrimiento Estrella: RHOG
RHOG apareció como un hit en múltiples búsquedas, y eso llamó la atención de los investigadores. Este gen codifica una GTPasa pequeña—una proteína que ayuda a transmitir señales dentro de las células. No es un checkpoint inmune clásico. No era parte de la lista de genes “obvios” que esperarías que mejoraran las CAR-T. Y precisamente por eso es tan emocionante.
Cuando eliminaron RHOG usando CRISPR, las CAR-T se transformaron completamente. Primero, se multiplicaron como nunca antes: 6 a 10 veces más que las CAR-T normales. Y esto no fue solo en células CD8+ (las asesinas clásicas), sino también en células CD4+ que normalmente funcionan más como ayudantes. Ambos tipos de células mostraron esta expansión masiva.
Pero aquí viene la parte realmente fascinante. Las CAR-T sin RHOG no solo se multiplicaron más—también cambiaron su comportamiento fundamental. Desarrollaron lo que se llama un fenotipo de memoria central, marcado por la expresión de CD62L y CD45RO. ¿Qué significa esto en términos prácticos? Imagina que tienes dos tipos de soldados: unos que pelean intensamente pero se agotan rápido (efectores), y otros que pelean de manera sostenida y pueden regenerarse (memoria central). Las CAR-T sin RHOG se convirtieron en el segundo tipo.
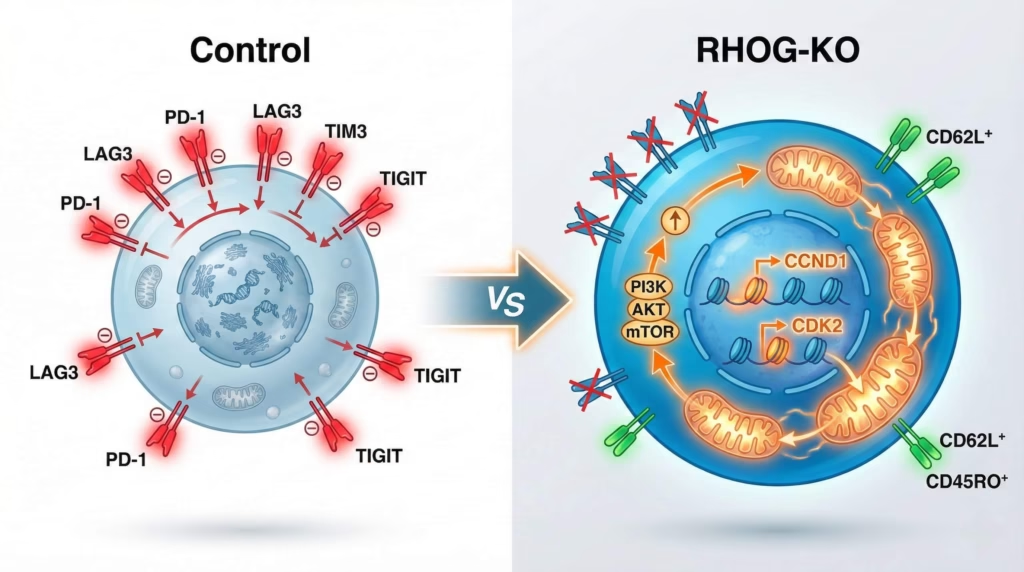
Los marcadores de agotamiento—esas proteínas que indican que las células están exhaustas—se redujeron drásticamente. LAG3, TIM3, TIGIT, PD-1: todos bajaron. Y lo mejor de todo es que a pesar de estos cambios, las CAR-T sin RHOG mantuvieron intacta su capacidad de matar células tumorales y producir citoquinas. No sacrificaron función por longevidad; obtuvieron ambas.
FAS: Deteniendo el Fraticidio
Mientras RHOG mejoraba la proliferación y reducía el agotamiento, los investigadores también miraron otro objetivo: FAS. Esta proteína es parte de una vía de muerte celular, y tiene un papel perverso en las terapias CAR-T.
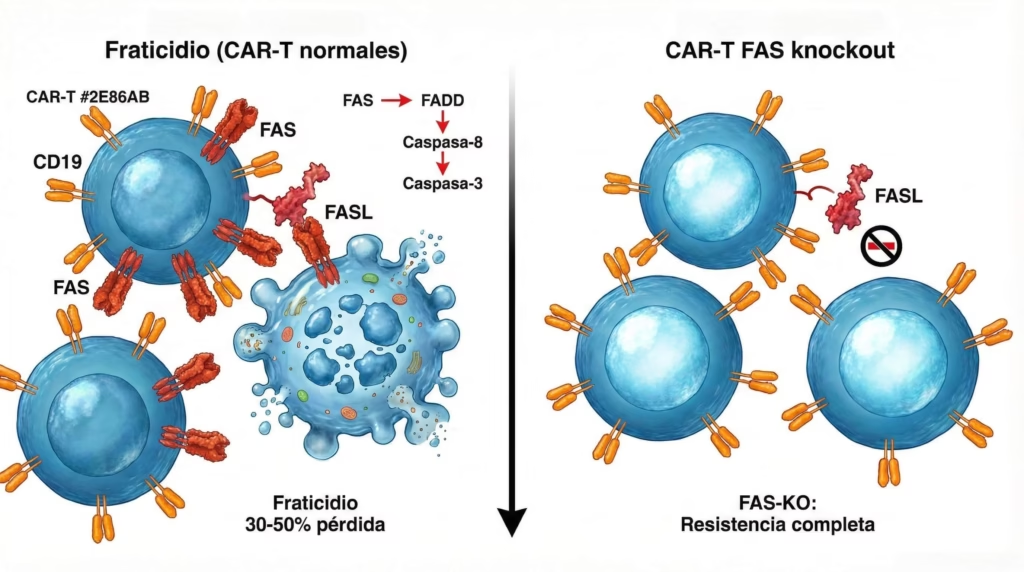
Funciona así: cuando una célula expresa FAS en su superficie y otra célula expresa FASL (el ligando de FAS), se unen y activan una cascada de muerte. Es como pulsar un botón de autodestrucción. Los tumores aprovechan esto expresando FASL para matar a las CAR-T que llegan a atacarlos. Pero el problema es aún peor porque las CAR-T también expresan tanto FAS como FASL, así que literalmente se matan entre sí.
Los investigadores pensaron: ¿y si simplemente eliminamos FAS? Sin el receptor, no hay forma de activar la vía de muerte, sin importar cuánto FASL haya en el ambiente. Y exactamente eso es lo que pasó.
Las CAR-T sin FAS dejaron de matarse entre sí. De repente, entre 30 y 50% más células sobrevivieron el proceso de manufactura y expansión inicial. Además, cuando estas células llegaron al tumor, el FASL expresado por las células cancerosas ya no podía matarlas. Era como quitarle el arma al enemigo. Y con más células vivas circulando en el cuerpo, el tratamiento se volvió más duradero y efectivo.
La Combinación Ganadora: RHOG + FAS
Aquí es donde la historia se pone realmente emocionante. Los investigadores se dieron cuenta de que RHOG y FAS atacan problemas diferentes: RHOG mejora la proliferación y reduce el agotamiento, mientras que FAS previene la muerte celular por fraticidio y ataque tumoral. ¿Qué pasaría si los combinaran?
El resultado fue sinérgico en el mejor sentido de la palabra. Las CAR-T con doble knockout (RHOG + FAS) se expandieron entre 12 y 15 veces más que las CAR-T normales. No fue simplemente aditivo (6X + algo de mejora); fue multiplicativo. Las dos modificaciones trabajaron juntas de manera complementaria.
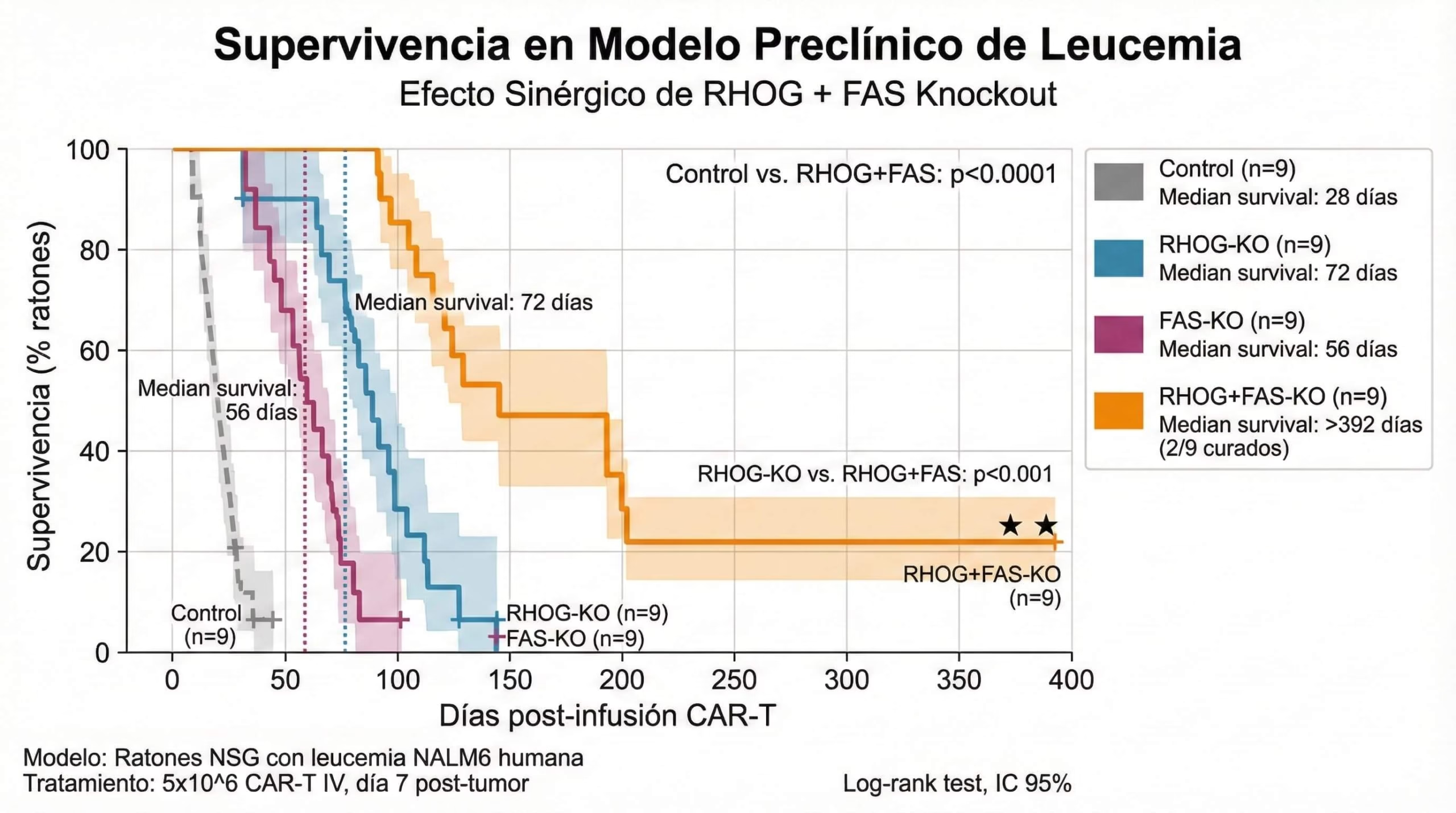
Pero lo verdaderamente impresionante vino cuando probaron estas células en ratones con leucemia NALM6, un modelo muy agresivo de cáncer. Los ratones control—sin tratamiento—murieron en 30 días. Los que recibieron CAR-T con solo RHOG knockout duraron hasta 60-80 días. Los que recibieron solo FAS knockout llegaron a 50-60 días. Pero los ratones tratados con CAR-T de doble knockout (RHOG + FAS) tuvieron resultados asombrosos: 2 de 9 ratones quedaron COMPLETAMENTE CURADOS y seguían vivos después de 392 días, más de un año después del tratamiento.
Déjame ponerlo en perspectiva. En investigación de cáncer, que 2 de 9 animales se curen completamente en un modelo tan agresivo es extraordinario. Y lo probaron en múltiples configuraciones de CAR—CAR-19 con señalización BBz, CAR-19 con señalización 28z, CAR-GD2 para neuroblastoma, CAR-GPC3 para hepatocarcinoma—y la combinación funcionó en todos.
CROP-seq In Vivo: Probando en Ratones Vivos
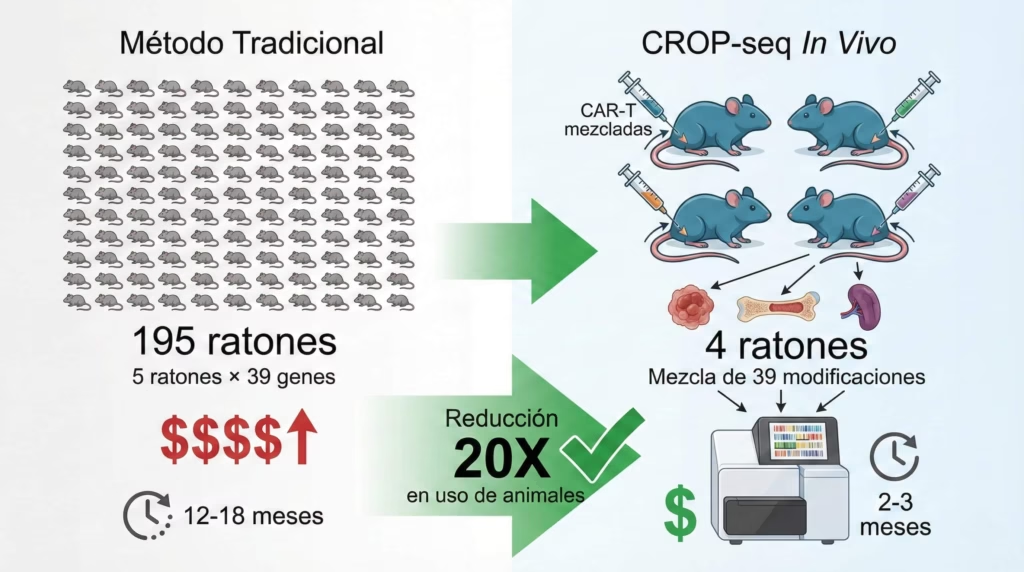
Ahora viene otra innovación metodológica que es casi tan importante como los descubrimientos mismos. Tradicionalmente, si quieres probar 39 genes diferentes para ver cuáles mejoran las CAR-T, necesitarías hacer 39 experimentos separados. Con 5 ratones por grupo para tener significancia estadística, estamos hablando de 195 ratones. Es caro, es lento, y requiere muchísimos animales.
Los investigadores desarrollaron algo llamado CROP-seq in vivo que cambia las reglas del juego. La idea es brillantemente simple: inyectan en un solo ratón una mezcla de CAR-T donde cada célula tiene un knockout diferente. Todas están marcadas con su guía CRISPR correspondiente como un código de barras molecular. Luego, después de un tiempo, recuperan células del tumor, la médula ósea y el bazo del ratón, y secuencian el ARN para ver qué modificaciones sobrevivieron y se expandieron mejor.
La clave técnica es que en lugar de leer el ADN de la guía CRISPR—que existe en solo dos copias por célula—leen el ARN mensajero de la guía, que se transcribe miles de veces. Esto da una señal mucho más fuerte y clara. Además, usan UMIs (unique molecular identifiers) para rastrear células individuales y sus expansiones clonales.
El resultado es una reducción de 20 veces en el uso de animales. Solo necesitaron 4 ratones para probar 39 genes diferentes. Y esto no solo es más ético—también es más rápido y más barato, lo que acelera enormemente el ritmo de descubrimiento. De hecho, RHOG, FAS, PRDM1 y CDKN2A fueron los top hits que emergieron de estos experimentos in vivo.
Edición de Bases: Alternativa Más Segura
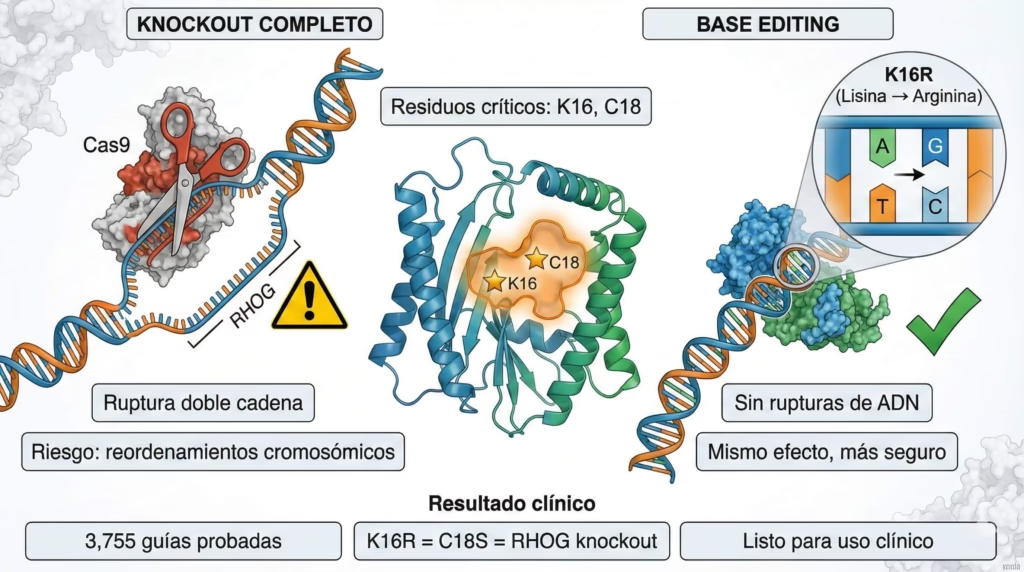
Los knockouts completos—donde eliminas un gen entero—funcionan perfectamente bien para investigación. Pero cuando piensas en llevar esto a pacientes reales, hay una consideración importante: cortar el ADN completamente puede causar rupturas de doble cadena que, aunque raras, pueden llevar a reordenamientos cromosómicos no deseados.
Aquí es donde entra la edición de bases, una tecnología más nueva y más precisa. En lugar de cortar el ADN, simplemente cambias una letra por otra: A→G o C→T. Es como usar corrector líquido en lugar de romper la página completa.
Los investigadores diseñaron 3,755 guías diferentes que “tildaban” todo el gen RHOG, buscando sistemáticamente qué cambios específicos reproducen el efecto del knockout completo. Probaron cuatro editores de bases diferentes (ABEmax, AncBE4max, SpRY-ABE, SpRY-CBE) para cubrir todas las posibilidades.
Y encontraron algo importante: mutaciones en los residuos Lys16 y Cys18, que están en el bolsillo de unión a GTP de la proteína RHOG, producen exactamente el mismo efecto que eliminar el gen completo. Cambios como K16R (lisina a arginina) o C18S (cisteína a serina) fueron suficientes. Esto es importante porque estas mutaciones missense—donde cambias un aminoácido por otro—son mucho más seguras para uso clínico que los knockouts completos. No generan rupturas de doble cadena, y el perfil de seguridad es mucho mejor.
Implicaciones Clínicas
Sé que probablemente te estás preguntando: ¿cuándo voy a ver esto en el hospital? La respuesta honesta es que tomará tiempo, pero el camino está bastante claro.
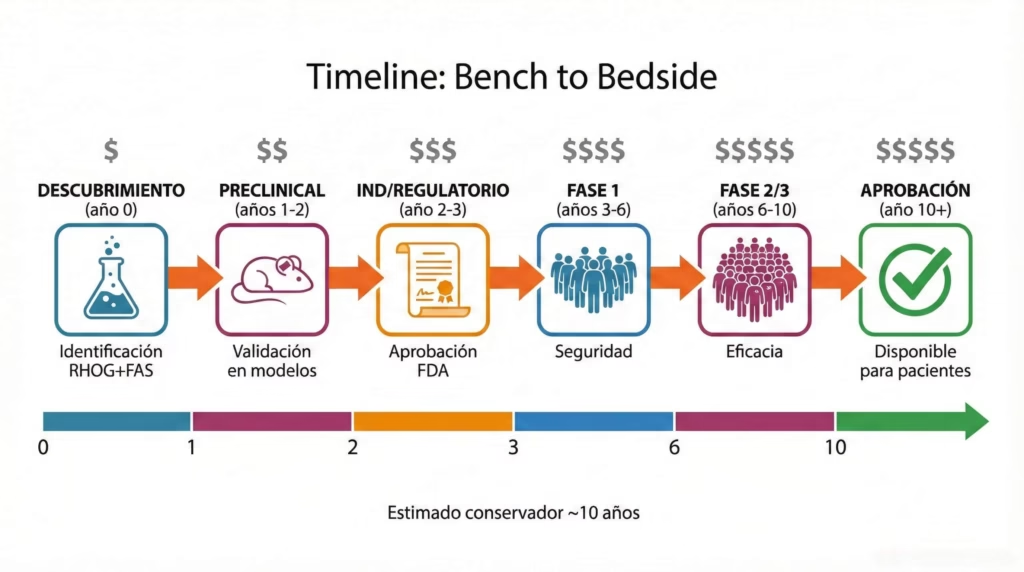
Primero necesitan 1-2 años adicionales de trabajo preclínico. Esto incluye validar los resultados en más modelos animales, probar diferentes tipos de tumores, optimizar los protocolos de manufactura, y hacer todos los estudios de toxicología que requiere la FDA. No es burocracia innecesaria—es asegurarse de que esto sea seguro antes de ponerlo en humanos.
Luego viene el proceso regulatorio, que toma alrededor de 6-12 meses. Aquí es donde los investigadores presentan una solicitud IND (Investigational New Drug) a la FDA con todos los datos preclínicos, protocolos de manufactura, y el diseño del ensayo clínico propuesto. La FDA revisa todo minuciosamente.
Una vez aprobado el IND, comienza la Fase 1, que dura típicamente 2-3 años. Aquí prueban principalmente seguridad en un pequeño grupo de pacientes (10-20 personas), usualmente pacientes que ya han fallado a todos los otros tratamientos disponibles. Empiezan con dosis bajas y van subiendo cuidadosamente mientras monitorean cualquier efecto adverso.
Si la Fase 1 muestra que es segura y hay señales de eficacia, avanzan a Fase 2 y 3, que toman otros 2-5 años combinados. Aquí prueban en grupos más grandes (50-200+ pacientes) comparando contra el tratamiento estándar actual. Necesitan demostrar no solo que funciona, sino que funciona mejor que lo que ya existe.
Sumando todo, estamos hablando de aproximadamente 10 años desde ahora hasta que esto podría estar aprobado y disponible para pacientes. Sé que suena como mucho tiempo, pero en el mundo de desarrollo de medicamentos, especialmente terapias celulares complejas, es en realidad bastante razonable.
¿Dónde lo veremos primero? Casi seguro en cánceres líquidos como leucemias y linfomas, porque las CAR-T ya están aprobadas para estos y hay infraestructura establecida. Los tumores sólidos serán el siguiente paso, y francamente son donde más se necesita porque ahí es donde las CAR-T actuales tienen más dificultades.
📝 Resumen (TL;DR)
Si solo vas a recordar algunas cosas de todo esto, que sean estas:
CELLFIE es una plataforma revolucionaria que combina CAR-T con edición CRISPR en un solo paso, permitiendo probar miles de modificaciones genéticas de manera masiva. Antes esto era imposible.
RHOG, un gen que nadie esperaba, resultó ser una estrella. Eliminarlo hace que las CAR-T se multipliquen 6-10 veces más, desarrollen memoria de larga duración, y resistan el agotamiento—todo sin perder su capacidad de matar el cáncer.
FAS knockout previene el fraticidio, ese fenómeno horrible donde las CAR-T se matan entre sí. Esto solo ya salva 30-50% más células, haciendo el tratamiento más efectivo.
La combinación RHOG + FAS es sinérgica, produciendo expansión de 12-15 veces y curando 2 de 9 ratones con leucemia agresiva por más de un año. Esto es extraordinario en modelos preclínicos.
CROP-seq in vivo reduce el uso de animales 20 veces, permitiendo probar 39 modificaciones genéticas en solo 4 ratones en lugar de 195. Esto acelera el descubrimiento y es más ético.
La edición de bases ofrece una alternativa más segura que los knockouts completos. Cambiar los residuos K16 y C18 en RHOG reproduce todos los beneficios sin generar rupturas de ADN de doble cadena.
El timeline clínico realista es de aproximadamente 10 años hasta aprobación completa, pero podríamos ver primeros ensayos en humanos en 2-3 años.
Referencias
Para más información respecto a este avance, visite el link. La información está en inglés.
Otros artículos relacionados:
- RhoG – RhoG’s Role in T Cell Activation and Function
- FAS – Evolutionary regulation of human Fas ligand (CD95L) by plasmin in solid cancer immunotherapy