Si tienes un familiar con diabetes tipo 2, probablemente alguien te ha dicho: “cuídate, porque eso es hereditario.” Y no están completamente equivocados. Pero tampoco están completamente en lo correcto.
La relación entre genética y diabetes tipo 2 (DT2) es uno de los temas más malinterpretados en medicina popular. La gente suele caer en uno de dos extremos: o creen que “les tocó por herencia” y poco pueden hacer, o ignoran completamente el componente genético. La realidad está en otro lugar, y la evidencia científica lo deja bastante claro.
En este post vamos a ver qué dice realmente la ciencia sobre el papel de los genes en la DT2, cuánto explican, cuánto no explican, y por qué el ambiente y el estilo de vida tienen un peso que los genes simplemente no pueden ignorar.
Primero: ¿la DT2 sí tiene un componente genético?
Sí. No vamos a negar lo que la evidencia muestra.
Los estudios en gemelos idénticos —que comparten el 100% de su ADN— muestran que si uno desarrolla DT2, el otro tiene entre 70% y 90% de probabilidad de desarrollarla también. Eso, comparado con gemelos fraternos (que comparten ~50% del ADN), apunta claramente a una influencia genética real.
Los estudios familiares también son consistentes: el riesgo de que un hermano desarrolle DT2 es aproximadamente 3 veces mayor que el de la población general.
Y los estudios de asociación del genoma completo (GWAS) han identificado más de 120 variantes genéticas asociadas a mayor riesgo de DT2, incluyendo genes como TCF7L2, KCNJ11, PPARG y FTO, que afectan la secreción de insulina y la sensibilidad a esta hormona.
Entonces sí: la genética importa. Pero aquí viene el problema.
El problema con “es hereditario”
Cuando la gente dice que la DT2 es hereditaria, asume que los genes son los responsables principales. Pero los datos no respaldan eso.
El análisis genómico de la meta-análisis más grande realizada hasta ahora solo logra explicar el 19% del riesgo de DT2. Dado que la heredabilidad estimada es de 30–70%, aproximadamente la mitad de esa heredabilidad genética sigue sin explicación.
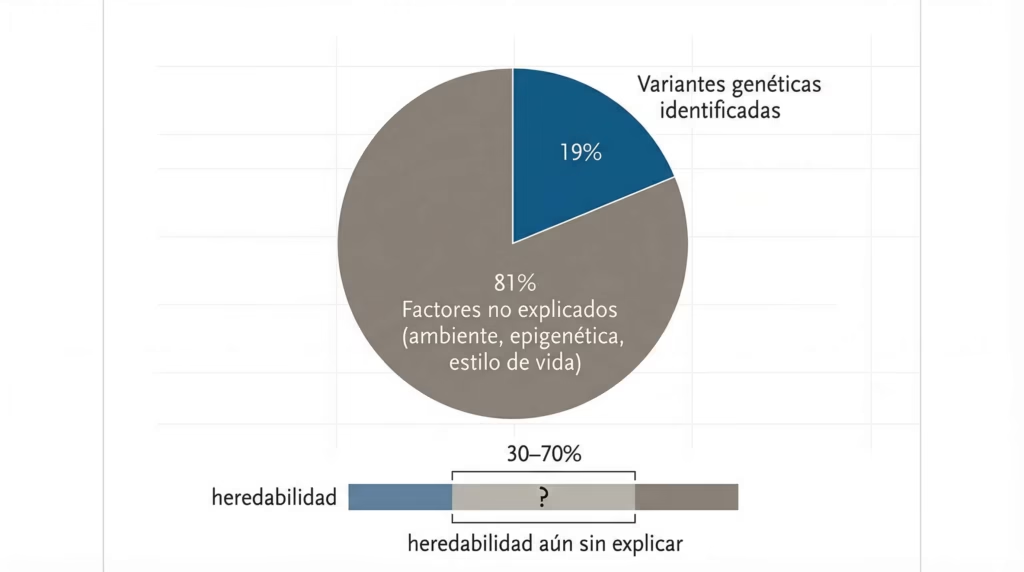
Dicho de forma más simple: incluso buscando en millones de genomas, los científicos solo pueden explicar una fracción pequeña del riesgo total. El resto lo atribuyen a factores ambientales, de estilo de vida, interacciones gen-ambiente, y epigenética.
Los factores de riesgo ambientales conocidos para DT2 incluyen obesidad, sedentarismo, bajo o alto peso al nacer, y estrés. Otros factores nutricionales y toxinas también pueden jugar un papel.
Hay otro punto que vale la pena mencionar: estudios recientes sugieren que los estudios en gemelos pueden estar sobreestimando la heredabilidad de la DT2, debido al ambiente compartido y efectos genéticos no aditivos, lo que genera una “heredabilidad fantasma.”
¿Por qué apareció la epidemia de DT2 apenas en los últimos 50 años?
Este es el argumento más contundente contra la narrativa de “es pura herencia.”
La epidemia de DT2 data apenas de los últimos 50 años. Es claro que en ese período solo el ambiente ha cambiado, no los genes. Sin embargo, la arquitectura genética determina cómo respondemos al ambiente: los variantes de riesgo podrían haber sido neutros o incluso beneficiosos antes de la adopción del estilo de vida occidental.

La hipótesis del “genotipo ahorrador” (thrifty genotype) propone que ciertos genes que favorecen el almacenamiento de energía fueron ventajosos en épocas de escasez de alimentos. Hoy, con acceso constante a alimentos procesados y estilos de vida sedentarios, esos mismos genes se vuelven un factor de riesgo. Los genes no cambiaron. El ambiente sí.
Lo que los estudios de intervención dejan muy claro
Aquí está la evidencia más directa y más relevante para el lector que pregunta: “¿y yo qué puedo hacer si tengo antecedentes familiares?”
Diabetes Prevention Program (DPP) — NEJM, 2002
Este estudio asignó aleatoriamente a 3,234 personas con glucosa elevada (prediabetes) a tres grupos: placebo, metformina, o intervención de estilo de vida (meta de 7% de pérdida de peso y 150 minutos de actividad física por semana). La intervención de estilo de vida redujo la incidencia de DT2 en un 58%, y metformina en un 31%, comparado con placebo. La intervención de estilo de vida fue significativamente más efectiva que metformina.
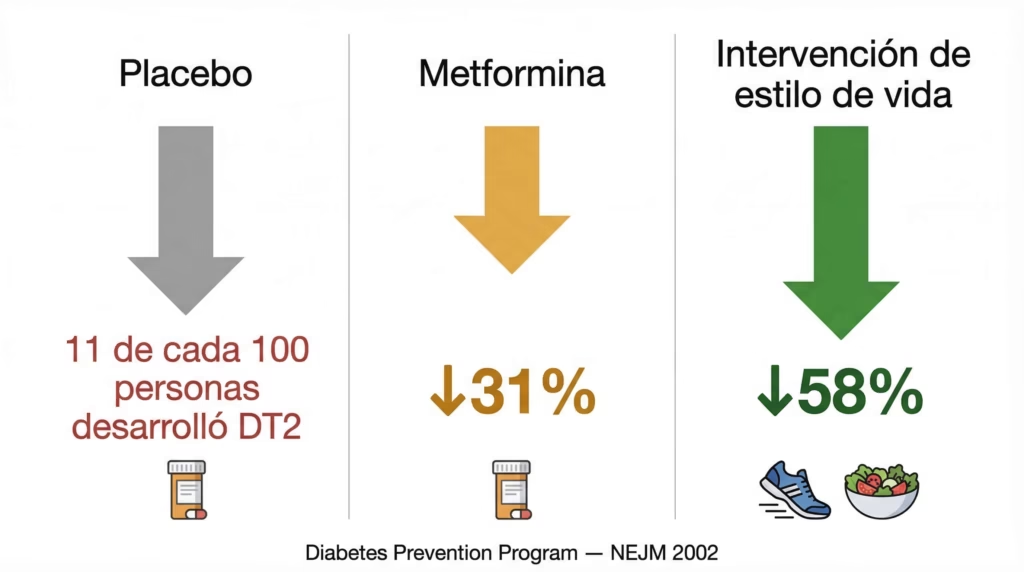
Pero más relevante aún para el tema de herencia: el riesgo poligénico para DT2 puede ser compensado por factores ambientales. El DPP mostró que la intervención de estilo de vida es efectiva incluso en el cuartil de participantes con mayor puntuación de riesgo poligénico para DT2. NCBI
Y el dato que más debería cambiar la narrativa popular: los efectos de la intervención de estilo de vida fueron mayores en quienes tenían variantes de alto riesgo en el gen TCF7L2, lo que sugiere que las personas con mayor susceptibilidad genética se benefician más, no menos, de los cambios en el estilo de vida.
Finnish Diabetes Prevention Study — NEJM, 2001
En 522 adultos de mediana edad con sobrepeso e intolerancia a la glucosa, una intervención individualizada de cambios en alimentación y actividad física redujo el riesgo de DT2 en un 58% durante 4 años. La reducción en la incidencia de diabetes se asoció directamente con los cambios en estilo de vida.
Nurses’ Health Study
Un estudio en 84,941 mujeres estimó que el 87% de los nuevos casos de DT2 en esa cohorte podrían haberse prevenido si todas las participantes hubieran tenido un perfil de bajo riesgo en los factores modificables: peso corporal, dieta, ejercicio, tabaquismo y consumo de alcohol.
87%. Eso es lo que el estilo de vida explica cuando se mide de forma poblacional.
¿Entonces para qué sirve saber si tienes genes de riesgo?
Buena pregunta. El conocimiento genético tiene utilidad, pero limitada.
Un estudio reportó que un resultado de “alto riesgo” en pruebas genéticas motivaría al 71% de los individuos sanos a adoptar cambios de estilo de vida. Sin embargo, un ensayo clínico aleatorizado mostró que el tamizaje genético para DT2, incluso acompañado de consejería genética, no cambió los comportamientos de salud ni los desenlaces de DT2, lo que sugiere que la información genética por sí sola no es suficiente para reducir el riesgo.
Saber que tienes genes de riesgo no te protege. Actuar sobre el estilo de vida, sí.
Epigenética: el puente entre genes y ambiente
Un punto que vale mencionar brevemente: la epigenética explica parte de por qué la DT2 “corre en familias” sin ser puramente genética.
Las familias comparten no solo genes, sino también patrones de alimentación, nivel de actividad física, exposición a estrés, y otros factores ambientales. Estos factores pueden modificar cómo se expresan los genes —sin cambiar el ADN— y esos cambios pueden transmitirse entre generaciones. Esto significa que lo que heredas no siempre es una mutación, sino a veces un patrón de expresión génica moldeado por el ambiente de tus padres.
Y los mexicanos, ¿qué?
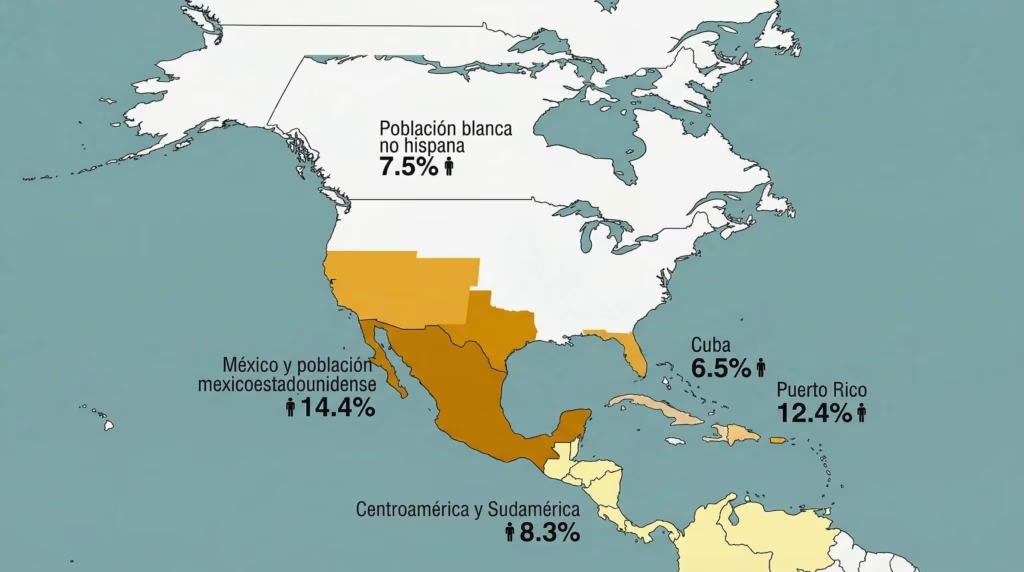
Entre las poblaciones latinas en Estados Unidos, los mexicanos tienen la prevalencia más alta de DT2: 14.4%, comparado con 12.4% en puertorriqueños, 8.3% en centroamericanos y sudamericanos, y 6.5% en cubanos.
En términos generales, los hispanos tienen tasas de DT2 hasta un 80% más altas que los blancos no hispanos, tanto en adultos como en niños.
¿Por qué? La respuesta no es solo genética.
La prevalencia elevada se explica parcialmente por factores socioculturales —como ingresos más bajos y menor acceso a educación y atención médica— así como por una susceptibilidad genética a la obesidad y una mayor resistencia a la insulina.
Hay variantes genéticas identificadas específicamente en mexicanos: el gen HNF1A está presente en el 2% de los mexicanos con DT2 pero solo en una décima parte de los individuos sanos, y conlleva un riesgo de 4 a 5 veces mayor de desarrollar la enfermedad.
Pero el punto clave sigue siendo el mismo: la prevalencia de DT2 diagnosticada y no diagnosticada es casi el doble en adultos de origen mexicano comparado con blancos no hispanos. BMC Endocrine Disorders Una brecha de ese tamaño no se explica solo con genética. El ambiente, la dieta, el acceso a servicios de salud, y la actividad física pesan de forma determinante.
DT1: mención breve
La diabetes tipo 1 es un caso distinto. Es una enfermedad autoinmune en la que el sistema inmune destruye las células beta del páncreas. Tiene un componente genético más definido (genes HLA-DR3/DR4), pero incluso en gemelos idénticos la concordancia es solo de ~50%, lo que indica que factores ambientales también activan la enfermedad. No es el enfoque de este post, pero vale aclarar que son mecanismos completamente diferentes.
Conclusión
La DT2 no es simplemente hereditaria, ni simplemente un problema de malos hábitos. Es una enfermedad donde los genes crean susceptibilidad, y el ambiente determina si esa susceptibilidad se convierte en enfermedad.
Lo que la evidencia muestra con claridad es:
- Los genes identificados hasta hoy explican menos del 20% del riesgo total.
- La epidemia de DT2 es de los últimos 50 años: los genes no cambiaron, el ambiente sí.
- Las intervenciones de estilo de vida reducen el riesgo en un 58%, incluso en personas con alta carga genética.
- Tener antecedentes familiares no es una sentencia. Es una señal de alerta que hace más relevante actuar sobre lo que sí se puede modificar.

Referencias
- Imamura M. Perspectives on genetic studies of type 2 diabetes from the GWAS era to precision medicine. Journal of Diabetes Investigation. 2024. doi:10.1111/jdi.14149
- Knowler WC, et al. (Diabetes Prevention Program Research Group). Reduction in the incidence of type 2 diabetes with lifestyle intervention or metformin. N Engl J Med. 2002;346(6):393–403.
- Tuomilehto J, et al. Prevention of type 2 diabetes mellitus by changes in lifestyle among subjects with impaired glucose tolerance. N Engl J Med. 2001;344(18):1343–1350.
- Hu FB, et al. Diet, lifestyle, and the risk of type 2 diabetes mellitus in women. N Engl J Med. 2001;345(11):790–797.
- Kreienkamp RJ, et al. Genetics of type 2 diabetes. In: Diabetes in America. NCBI Bookshelf. 2023. NBK597726.
- Prasad RB, Groop L. Genetics of type 2 diabetes—pitfalls and possibilities. Genes (Basel). 2015;6(1):87–123. PMC4377835
- Armstrong ND, et al. Variant level heritability estimates of type 2 diabetes in African Americans. Sci Rep. 2024;14:14009
- Billings LK, Florez JC. The genetics of type 2 diabetes: what have we learned from GWAS? Ann N Y Acad Sci. 2010;1212:59–77. PMC3057517
- Prokopenko I, McCarthy MI, Lindgren CM. Type 2 diabetes: new genes, new understanding. Trends Genet. 2008;24(12):613–621
- NIDDK. The Diabetes Prevention Program and its outcomes study. Diabetes Care. 2024. PMC12178622.
- Mainous AG 3rd, et al. Type 2 diabetes mellitus in Latinx populations. Mayo Clin Proc Innov Qual Outcomes. 2022. PMC9009996
- Caballero AE. Understanding the growing epidemic of type 2 diabetes in the Hispanic population. Curr Diab Rep. 2005. PMC6953173
- Morales J, et al. Understanding the impact of five major determinants of health on type 2 diabetes in U.S. Hispanic/Latino families: Mil Familias. BMC Endocr Disord. 2020;20(1):4
VIDEO
Si prefieres ver este tema en formato visual, tenemos el video disponible en nuestro canal de YouTube y en TikTok. @pormeracuriosidad.

AVISO LEGAL
El contenido de este artículo es exclusivamente informativo y de divulgación científica. No sustituye la consulta médica profesional, el diagnóstico ni el tratamiento. Si tienes dudas sobre tu salud o la de un familiar, consulta a tu médico. Las referencias citadas corresponden a estudios publicados en revistas científicas revisadas por pares.


